
Termologia
Propagação do calor
01-(UNIFOR- Medicina – CE-019)



02-(UNESP-SP-018)

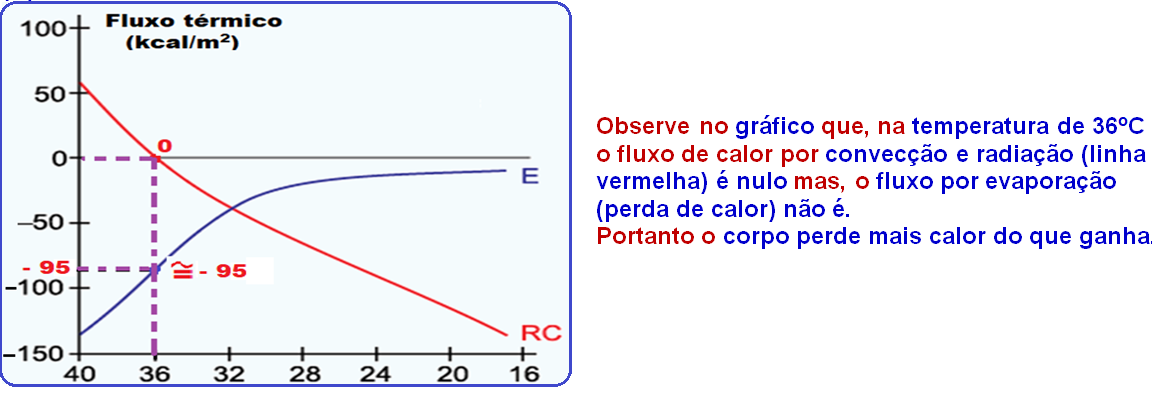
O gráfico mostra o fluxo térmico do ser humano em função da temperatura ambiente em um experimento no qual o metabolismo basal foi mantido constante.
A linha azul representa o calor trocado com o meio por evaporação (E) e a linha vermelha, o calor trocado com o meio por radiação e convecção (RC).

Sabendo que os valores positivos indicam calor recebido pelo corpo e os valores negativos indicam o calor perdido pelo corpo, conclui-se que:
(A) em temperaturas entre 36 ºC e 40 ºC, o corpo recebe mais calor do ambiente do que perde.
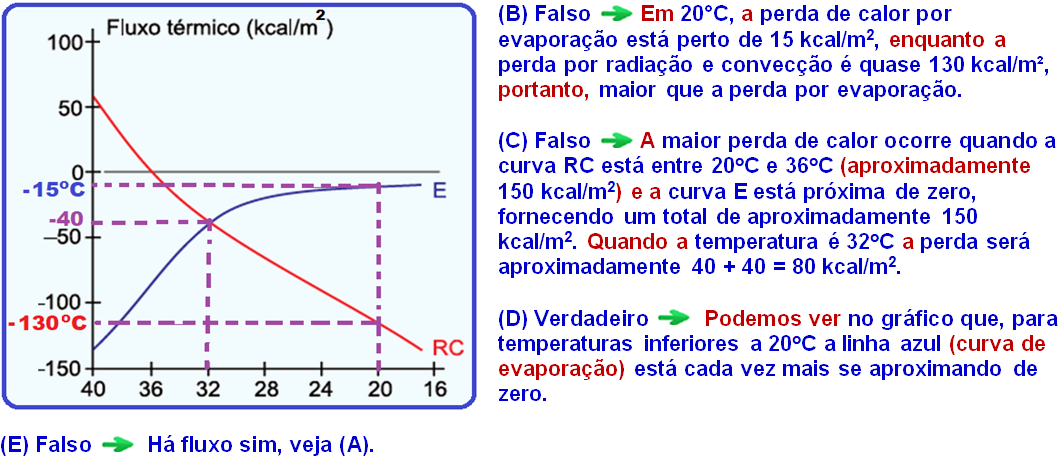
(B) à temperatura de 20 ºC, a perda de calor por evaporação é maior que por radiação e convecção.
(C) a maior perda de calor ocorre à temperatura de 32 ºC.
(D) a perda de calor por evaporação se aproxima de zero para temperaturas inferiores a 20 ºC.
(E) à temperatura de 36 ºC, não há fluxo de calor entre o corpo e o meio.
03-(UNICAMP-SP-018)

Mesmo em manhãs bem quentes, é comum ver um cão tomando sol.
O pelo do animal esquenta e sua língua do lado de fora sugere que ele está cansado.
O pelo do animal está muito quente, mas mesmo assim o cão permanece ao sol, garantindo a produção de vitamina D3.
Durante essa exposição ao sol, ocorrem transferências de energia entre o cão e o ambiente, por processos indicados por números na figura abaixo.

(Adaptado de KHAN ACADEMY, Endotherms and ectotherms. Disponível em www.khanacademy.org. Acessado em 26/07/17.)
Em ordem crescente, os números correspondem, respectivamente, aos processos de
a) convecção, evaporação, radiação, condução e radiação.
b) convecção, radiação, condução, radiação e evaporação.
c) condução, evaporação, convecção, radiação e radiação.
d) condução, radiação, convecção, evaporação e radiação.
04-(FUVEST-SP-018)

Um fabricante de acessórios de montanhismo quer projetar um colchão de espuma apropriado para ser utilizado por alpinistas em regiões frias.
Considere que a taxa de transferência de calor ao solo por uma pessoa dormindo confortavelmente seja 90 kcal/hora e que a transferência de calor entre a pessoa e o solo se dê exclusivamente pelo mecanismo de condução térmica através da espuma do colchão.
Nestas condições, o gráfico representa a taxa de transferência de calor, em J/s, através da espuma do colchão, em função de sua espessura, em cm.

Considerando 1 cal = 4 J, a menor espessura do colchão, em cm, para que a pessoa durma confortavelmente é
![]()
05-Universidade Estadual de Maringá (UEM) – 019

Ao despertar no castelo do conde Drácula com o dia já prestes a raiar, seu hóspede Jonathan Harker

registrou em seu diário: “Dormi até tarde e só despertei de livre e espontânea vontade quando meu sono terminou. Depois de trocar de roupa, passei do quarto para a outra sala, onde havia ceado na noite anterior. Encontrei um desjejum de pratos frios, acompanhado de café bem quente, cuja temperatura fora mantida [constante] por ter sido colocado junto da lareira a fim de não perder o calor.” (Adaptado de STOKER, B. Drácula. São Paulo: Nova Cultural, 2002, p. 26).
Em relação à temperatura do café, conforme descrição do fragmento, e aos processos de transmissão de calor, assinale o que for correto.
01) A temperatura do café permanece constante porque a quantidade de calor que ele recebe é a mesma que ele perde.
02) A temperatura do café permanece constante, independentemente da distância em que ele se encontra da lareira.
04) Uma maneira de a energia térmica proveniente da lareira se propagar ocorre na forma de radiação eletromagnética.
08) Se o café for afastado da posição em que foi colocado junto à lareira, sua temperatura diminuirá.
16) A informação de que a temperatura do café se mantém constante é equivocada, pois é impossível que isso ocorra na prática.
06-Instituto Federal de Educação, Ciência e Tecnologia do Paraná (IFPR) – 2019

A temperatura do nosso corpo é normalmente mantida em torno de 36 ºC, enquanto a do ambiente é, em geral, inferior a este valor.

Analise as sentenças abaixo, a partir da informação e das imagens acima.
I) Se a temperatura ambiente for muito baixa, a transmissão de calor do corpo para o ambiente se faz com muita rapidez provocando a sensação de frio.
II) Um bom agasalho para o inverno é aquele que impede que o frio passe através dele.
III) Os agasalhos de lã atenuam a sensação de frio, porque são feitos de materiais isolantes térmicos, reduzindo assim a quantidade de calor, que é transmitida de nosso corpo para o exterior.
IV) Em dias de frio, pássaros e gatos ficam com penas e pelos eriçados. Isso mantém, entre penas ou pelos, camadas de ar aquecido, que é um bom isolante térmico.
Estão corretas apenas:
A) I e III.
B) I, III e IV.
C) I, II e III.
D) II e IV.
07-(Faculdade de Medicina de Jundiaí “FMJ” –SP – 018)



No Sistema Internacional de Unidades, o coeficiente de condutividade térmica pode ser expresso na unidade
![]()
08-(Universidade Estadual do Paraná (UNESPAR) – 019)

Depois de ministrar o conteúdo sobre calor e temperatura, o professor divide os alunos em 4

grupos para que elaborem um resumo sobre suas principais conclusões a respeito dos fundamentos desses conceitos.
I. Sabemos que calor é uma das formas de energia que se propaga na forma de ondas eletromagnéticas. Num meio material, o calor pode se propagar por condução ou convecção. Os termômetros medem o grau de agitação das moléculas, grandeza que caracteriza a temperatura do corpo;
II. O termômetro é um instrumento que quantifica o calor contido num corpo. Quanto maior a temperatura do corpo, mais calor ele tem armazenado. Quando o corpo com mais calor entra em contato com outro com quantidade menor de calor, observa-se uma troca de calor entre eles;
III. O calor é uma energia em trânsito em função da diferença de temperatura entre 2 ou mais corpos. O calor flui do corpo com menor temperatura para o corpo que apresenta maior temperatura. Os termômetros no Brasil utilizam a escala Celsius, que é dividida por 180;
IV. A temperatura absoluta do corpo, dada na escala Kelvin, é obtida através de um termômetro a gás que mede o calor propagado pelo corpo. Ou seja, apenas o termômetro a gás mede o calor absoluto do corpo.
Assinale a alternativa que apresenta o(s) resumo(s) com conceitos CORRETOS.
a) Apenas I;
b) Apenas II e IV;
c) Apenas I, III e IV;
d) Apenas IV;
e) Todos os resumos estão corretos
Termometria
09-(ENEM-MEC-017)


Calorimetria (calor sensível, calor latente e trocas de calor)
10-(FPS-Faculdade Pernambucana de Saúde-PE-2019)


11-(UFAM-AM-2019)



12-(UFRR-RR-019)


13-(Faculdade de Tecnologia Termomecânica – SP- 019)

Com o propósito de medir a temperatura de um forno, um fragmento de ferro é inserido em seu interior, sendo aí deixado um tempo suficiente para que entre em equilíbrio térmico com o forno.

Num dado momento, o fragmento é retirado do forno e rapidamente jogado dentro de um calorímetro ideal, contendo água inicialmente a 20 ºC e com uma massa igual à do fragmento de ferro. O calor específico do ferro é 0,12 cal/(g.ºC) e da água é 1,0 cal/(g.ºC).
Após certo tempo, verifica-se que a temperatura de equilíbrio térmico entre o ferro e a água é igual a 80 ºC.
Sabendo que durante a passagem do forno para o calorímetro não houve variação de temperatura no fragmento de ferro e que a troca de calor ocorreu apenas entre o ferro e a água, a alternativa que indica corretamente a temperatura do forno é:
(A) 320 ºC. (B) 410 ºC. (C) 460 ºC. (D) 540 ºC. (E) 580 ºC
14-(UNICAMP-SP-018)


15-(Faculdade de Medicina de Taubaté – FMT – 019)

Um agitador é usado para aquecer uma certa quantidade de água, contida num recipiente termicamente isolado.
Considere que o calor específico da água é 1 cal/(g.oC).
Admitindo que 1 cal = 4,2 J, determine a variação de temperatura sofrida por uma massa de água de 400 g que recebe desse agitador 4,2.104 J de energia.
a) 25,0 graus Celsius
b) 52,0 graus Celsius
c) 22,0 graus Celsius
d) 55,0 graus Celsius
e) 2,50 graus Celsius
16-(FGV-RJ-019)


17-(FGV-RJ-019)


18-(Faculdade de Medicina do Hospital Israelita Albert Einstein-SP-018)



![]()
19-(UNIFESP-SP-018)


20-(FAMERP-SP-018)


21-(PUC – RIO – 019)

Dentro de um calorímetro perfeito, de capacidade C = 40 cal/oC e temperatura inicial 0 oC, colocam-se 100 g de um material de calor específico 0,50 cal/goC a uma temperatura de 90 oC, e uma massa de 10 g de gelo a 0 oC.

Calcule, em oC, o valor da temperatura final de equilíbrio do sistema.
Dados: CÁGUA = 1,0 cal/go C LFUSAO GELO = 80 cal/g
A) 40 B) 39 C) 38 D) 37 E) 36
22-(PUC-SP-018)


23-(UDESC-SC-019)

Um copo contendo 200ml de água foi colocado no refrigerador até que a temperatura atingisse 5ºC negativos.

O copo foi, então, retirado do refrigerador e colocado sobre uma mesa, em uma cozinha cuja temperatura ambiente estava 10ºC.
Assinale a alternativa que corresponde ao calor total recebido pela água até atingir o equilíbrio térmico.
( ) 1,5kcal B. ( ) 16,5kcal C. ( ) 18,5kcal D. ( ) 19,5kcal E. ( ) 4,1kcal
Dilatometria
24-(Faculdade de Tecnologia do Estado de São Paulo – FATEC – 019)

Em uma aula de laboratório de calorimetria, uma aluna da Fatec precisa determinar o calor específico de um material desconhecido de massa 1,0 kg.
Para isso, ele usa, por 1 min, um forno elétrico que opera em 220 V e 10 A.

Após decorrido esse tempo, ele observa uma variação de temperatura de 220 °C. Considerando que o forno funciona de acordo com as características apresentadas, podemos afirmar que o calor específico determinado, em J/kg·K, foi de
(A) 4,2.103
(B) 8,4.102
(C) 6,0.102
(D) 4,9.102
(E) 1,5.102
25-(UDESC-SC-019)

Considere
um recipiente
de volume v cujo coeficiente de dilatação volumétrica
é ![]() R. Um líquido
de coeficiente de dilatação volumétrica
R. Um líquido
de coeficiente de dilatação volumétrica ![]() l é
colocado no recipiente até enchê-lo completamente. Após
l é
colocado no recipiente até enchê-lo completamente. Após

uma
variação de temperatura ![]() t,
o recipiente e o líquido têm seus volumes dilatados, e transborda
um volume
t,
o recipiente e o líquido têm seus volumes dilatados, e transborda
um volume ![]() de
líquido.
de
líquido.
Assinale
a alternativa que corresponde ao valor (![]() l –
l – ![]() R ).
R ).![]() t.
t.
A. ( ) 0,2 B. ( ) 10 C. ( ) 5 D. ( ) 0,1 E. ( ) 2
Resolução
Comentada – Termologia – 2019/2018
01-
. Correta São três os processos de propagação de calor:
Convecção térmica
Trata-se da transferência de energia térmica (calor) pela matéria em movimento devido à diferença de densidades dessa matéria.
Condução térmica
O calor é conduzido de um ponto a outro do corpo sem que haja deslocamento das partículas.
Irradiação térmica
A irradiação (ou radiação) térmica é uma das formas de propagação do calor que ocorre por meio de ondas eletromagnéticas, chamadas de ondas de calor.
II. Correta
III. Correta – O hipotálamo possui outra ação importante: funciona como autêntico termostato, regulando o aumento ou a perda de calor pelo corpo. Os responsáveis pelo equilíbrio térmico parecem ser certos núcleos celulares de dois tipos diferentes. Um relaciona-se com a perda de calor verificada no organismo: se a temperatura aumenta, sua função é promover alterações respiratórias, transpiração, dilatação dos vasos sanguíneos e diminuição das atividades metabólicas. O outro tipo relaciona-se com a conservação do calor, produzindo os efeitos contrários, a fim de compensar a queda de temperatura.
IV – Falsa devem utilizar materiais que são bons isolantes térmicos (baixas e não altas condutividades térmicas) como, por exemplo, lã, algodão, peles de alguns animais.
R- E
02-
A Taxa de Metabolismo Basal é a quantidade mínima de energia (calorias) necessária para manter as funções vitais do organismo em repouso.
(A) Falsa
R- D
03-
01- 1.
Condução ![]() O calor, devido
ao contato
entre o cão e chão, é conduzido do solo
para o cão, sem que
haja deslocamento
das partículas.
O calor, devido
ao contato
entre o cão e chão, é conduzido do solo
para o cão, sem que
haja deslocamento
das partículas.
2.
Evaporação ![]() A língua do
cão libera
calor para
o meio ambiente pela
evaporação da saliva.
A língua do
cão libera
calor para
o meio ambiente pela
evaporação da saliva.
3.
Convecção ![]() Trata-se
da transferência
de energia térmica (calor)
pela matéria (no
caso, ar) em movimento
devido à diferença de densidades, ou de temperatura, dessa matéria
(ar).
Trata-se
da transferência
de energia térmica (calor)
pela matéria (no
caso, ar) em movimento
devido à diferença de densidades, ou de temperatura, dessa matéria
(ar).
O cão transfere calor para o ar próximo aquecendo-o, ficando mais leve e subindo, originando correntes de convecção.
4.
Radiação ![]() Fenômeno
no qual a energia
emitida pelo Sol chega até a Terra pelo vácuo através
das ondas
eletromagnéticas, inclusive o infravermelho (radiação térmica).
Fenômeno
no qual a energia
emitida pelo Sol chega até a Terra pelo vácuo através
das ondas
eletromagnéticas, inclusive o infravermelho (radiação térmica).
5.
Radiação ![]() Radiação
térmica (infravermelho,
ondas de calor) são emitidas
do corpo do cão para
o meio
ambiente.
Radiação
térmica (infravermelho,
ondas de calor) são emitidas
do corpo do cão para
o meio
ambiente.
R- C
04-

R- B
05-
01. Correto – calor é energia em trânsito, transferida de um corpo de maior temperatura para outro de menor temperatura e, para que a temperatura do café permaneça constante a quantidade de calor que ele recebe deve ser a mesma que ele perde.
02. Falso – à medida que ele se afasta da lareira vai recebendo menos calor da mesma e sua temperatura vai diminuindo.
04. Correto
– 
08- Correto – veja 02.
16 – Falso – veja 01
R – (01 + 04 + 08) = 13
06-
I. Correta – quanto maior a diferença de temperatura entre os dois corpos mais rápida será a transferência de calor do corpo de maior para o de menor temperatura.
II. Falsa – quem se transfere é o calor (veja I)
III. Correta.
IV- Correta – No frio, a aves costumam eriçar suas penas para captar o ar entre eles e se aquecerem, ficando mais “gordinhos” e mantendo uma pequena camada de ar sobre seus corpos.

Para adaptar-se ao frio, mamíferos (como nós) e aves eriçam seus pelos ou penas (quer dizer arrepiam-se!).
Isto acontece porque o arrepio faz aumentar o isolamento térmico. Quanto mais pelos ou penas o animal tiver, melhor será esse sistema de proteção.
R- B
07-

08-
I. Correta – O calor é uma das formas de radiação eletromagnética (principalmente a radiação infravermelha). Num meio material, o calor pode se propagar por condução ou convecção e não por irradiação que ocorre também no vácuo. Temperatura corresponde a um número que mede o grau de vibração (agitação das moléculas).
II. Falsa – o termômetro é um instrumento que mede a temperatura (grau, nível de agitação) das moléculas de um corpo.
III. Falsa – a escala Celsius é dividida por 100.
IV. Falsa – o termômetro a gás, baseado na variação de volume do gás mede apenas pequenas variações de temperatura.
R- A
09-

10-


11-
Observe pelo enunciado que a substância é a mesma (alumínio), mas não fez referência às massas, que podem ser diferentes.
O calor específico depende somente da substância, não da quantidade de massa, pois ele é definido com a quantidade de calor necessária para elevar uma unidade de massa de um grau Celsius (ou Kelvin, ou Fahrenheit). A capacidade térmica, além de depender do calor específico da substância, depende da massa do corpo. Portanto trata-se da capacidade térmica.
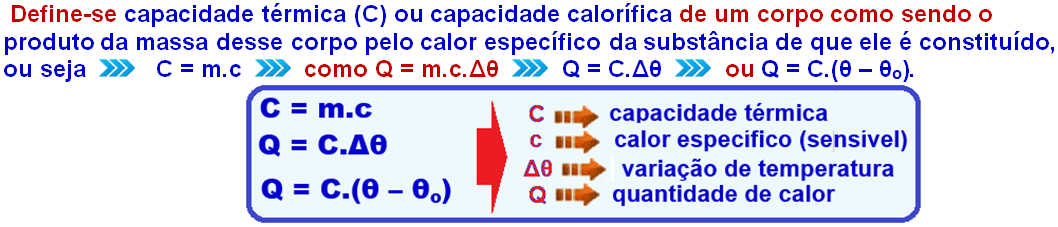
Capacidade térmica (C)
Define-se capacidade
térmica (C) ou capacidade calorífica de
um corpo como sendo o produto
da massa desse corpo pelo calor específico da substância de que ele
é constituído, ou seja ![]() C = m.c
C = m.c ![]() como Q = m.c.Δθ
como Q = m.c.Δθ ![]() Q
= C.Δθ
Q
= C.Δθ ![]() ou Q
= C.(θ – θo).
ou Q
= C.(θ – θo).


R – B
12-
Princípio da Conservação da energia (trocas de calor)
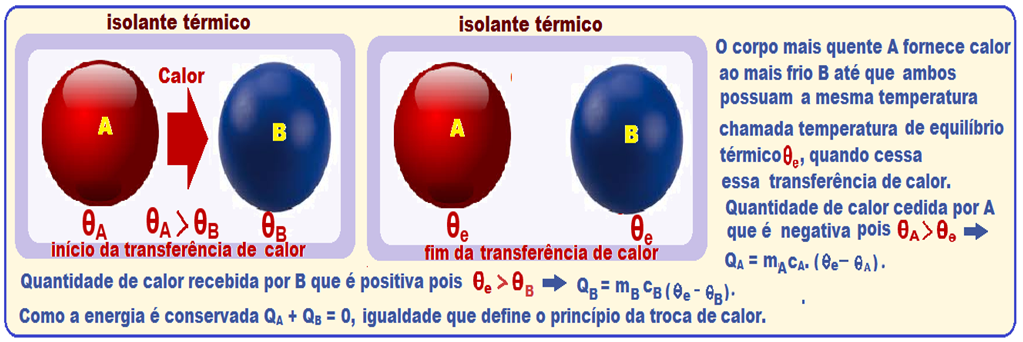
Capacidade térmica (C)

R- A
13-
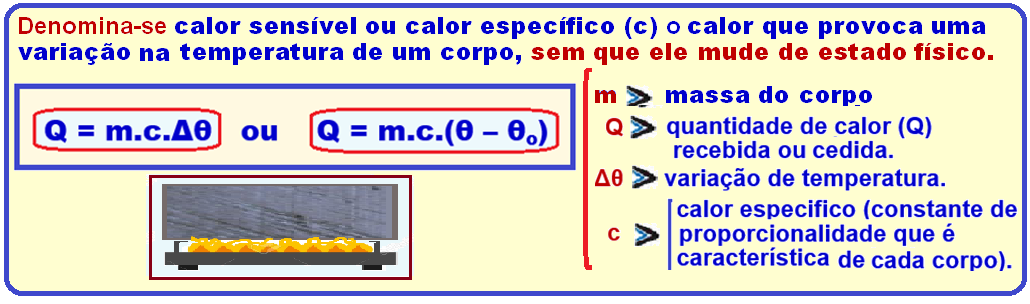
Equação fundamental da calorimetria (calor sensível ou calor específico)
Princípio da Conservação da energia
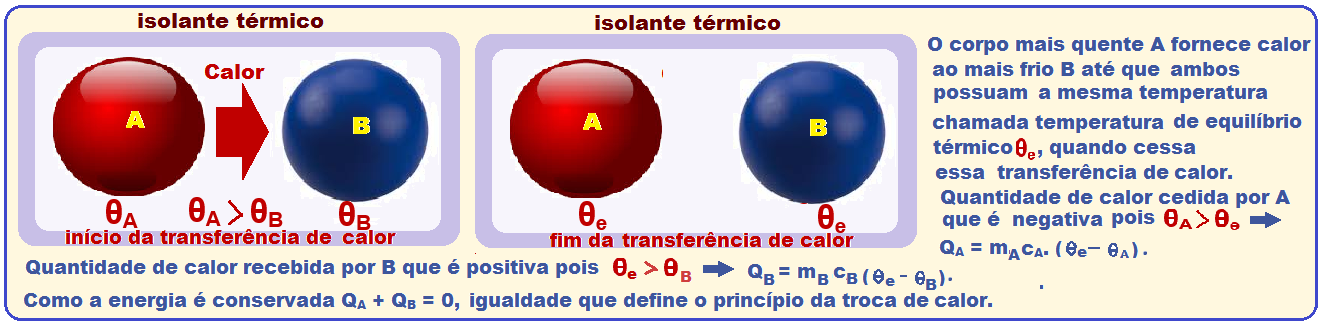
A
teoria acima é válida
para mais de um corpo e,
como a quantidade de calor recebida
é positiva e a cedida é negativa, tem-se que ![]() Q1 + Q2 + Q3 + …. + QN = 0 ou
m1.c1.(θe –
θ1) + m2.c2.( θe – θ2) + m3.c3.( θe – θ3) + … +
mN.cN.( θe –
θN)
= 0.
Q1 + Q2 + Q3 + …. + QN = 0 ou
m1.c1.(θe –
θ1) + m2.c2.( θe – θ2) + m3.c3.( θe – θ3) + … +
mN.cN.( θe –
θN)
= 0.
Enunciado desse princípio das trocas de calor:

Seja to a temperatura inicial do pedaço de ferro dentro do forno e no início da troca de calor com a água do calorímetro e, pelo enunciado mágua = mferro = m com tequilíbrio = 80 oC e toágua = 20 oC.
Quantidade
de calor recebido pela massa m de água ![]() Qágua =
m.cágua (tequilíbrio – toágua)
= m.1.(80 – 20)
Qágua =
m.cágua (tequilíbrio – toágua)
= m.1.(80 – 20) ![]() Qágua =
60m.
Qágua =
60m.
Quantidade
de calor cedido pela massa m ferro ![]() Qferro =
m.cferro (tequilíbrio – to) =
m.0,12.(80 – to)
Qferro =
m.cferro (tequilíbrio – to) =
m.0,12.(80 – to) ![]()
Qferro = 9,6m – 0,12mto.
Qágua +
Qferr = 0 ![]() 60m
+ 9,6m – 0,12mto = 0
60m
+ 9,6m – 0,12mto = 0 ![]() to =
69,6m/0,12m
to =
69,6m/0,12m ![]() to =
580 oC.
to =
580 oC.
R- E
14-
São
fornecidos: Volume
de água ![]() V
= 500 L; Variação
de temperatura da água
V
= 500 L; Variação
de temperatura da água ![]() ∆t
= (47
– 20) = 27 oC; Densidade
da água
∆t
= (47
– 20) = 27 oC; Densidade
da água ![]() d
= 1 kg/L; Calor
específico da água
d
= 1 kg/L; Calor
específico da água ![]() c =
4 kJ/kgoC =
4.103 J/kgoC e
c =
4 kJ/kgoC =
4.103 J/kgoC e
1 kWh = 3,6.106 J.

15-
W = Q = 4,2.104 j/4,2 = 104 cal.
Q =
m.c ∆t ![]() 104 =
400.1.∆t
104 =
400.1.∆t ![]() ∆t
= 10000/400
∆t
= 10000/400 ![]() ∆t
= 25 o C.
∆t
= 25 o C.
R- A
16-

17-

R- D
18-


R- D
19-

b) São dados:


20-


21-
Recipiente
passando de to = 0 oC até te ![]() Q1 =
C.(te – to) =
40.(te – 0)
Q1 =
C.(te – to) =
40.(te – 0) ![]() Q1 =
40te
Q1 =
40te
Material
passando de to = 90 oC até te ![]() Q2 m.c
.(te – to)
= 100.0,5.(te – 90)
Q2 m.c
.(te – to)
= 100.0,5.(te – 90) ![]() Q2 =
50te – 4500
Q2 =
50te – 4500
Gelo
a 0 oC se fundindo (passando
de gelo a 0oC até água a 0oC) ![]() Q3 =
m.L =
10.80
Q3 =
m.L =
10.80 ![]() Q3 =
800 cal
Q3 =
800 cal
Água
passando de to = 0oC até te ![]() Q4 =
m.c.(te – to) =
10.1.(te – 0)
Q4 =
m.c.(te – to) =
10.1.(te – 0) ![]() Q4 =
10te.
Q4 =
10te.
Como
o calorímetro
é perfeito não
hà trocas de calor com o meio exterior e a soma
das quantidades de calor trocadas entre eles deve ser nula ![]() 40te +
50te – 4500 + 800 + 10te =
0
40te +
50te – 4500 + 800 + 10te =
0 ![]() 100te =
3700
100te =
3700 ![]()
te =
3700/100 ![]() te =
37 oC.
te =
37 oC.
R- D
22-

23-
São dados: dágua = 1000 kg/m3; cgelo = 0,5 cal/goC; cágua = 1 cal/goC; Lfusão = 80 cal/g.
Vágua = 200 ml = 0,2l = 0,2 dm3 = 0,2.10-3 m3.
dágua =
m/V ![]() 103 kg/m3 =
m/0,2.10-3 m3
103 kg/m3 =
m/0,2.10-3 m3 ![]() m =
0,2 kg =
200 g
m =
0,2 kg =
200 g
De
gelo a – 5oC até gelo a 0oC ![]() Q1 =
m.cgelo.
Q1 =
m.cgelo.![]() =
200.0,5.(0 – (-5)) =
500 cal.
=
200.0,5.(0 – (-5)) =
500 cal.
De
gelo a 0oC até água a 0oC ![]() Q2 =
m.Lfusão =
200.80 =
16000 cal.
Q2 =
m.Lfusão =
200.80 =
16000 cal.
De
água a 0oC até água a 10 oC ![]() Q3 =
m.cágua.(10 – 0) =
200.1.10 =
2000 cal.
Q3 =
m.cágua.(10 – 0) =
200.1.10 =
2000 cal.
Qtotal = 500 + 16000 + 2000 = 18500 cal = 18,5 kcal.
R- C
24-
Dilatação linear dos sólidos
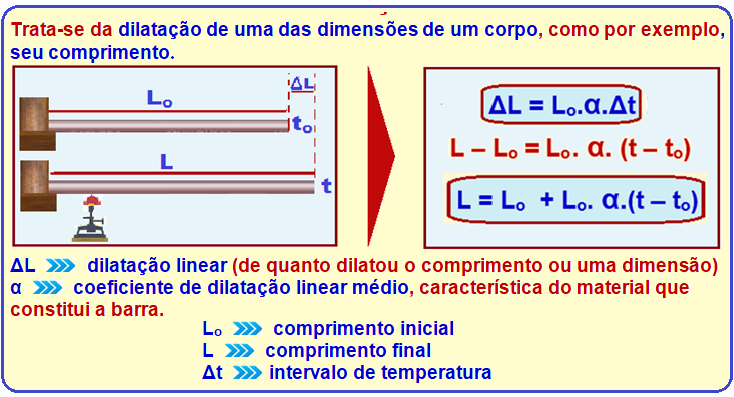
Pelo gráfico Lo = 80 cm (L quando T = 0oC) e quando T = 100 oC, L = 80,16 cm.
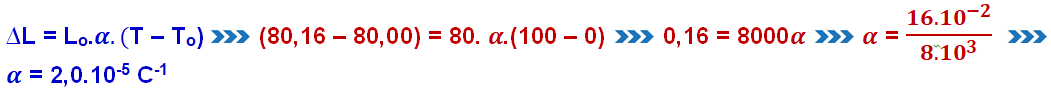
R- C
25-
Dilatação dos líquidos
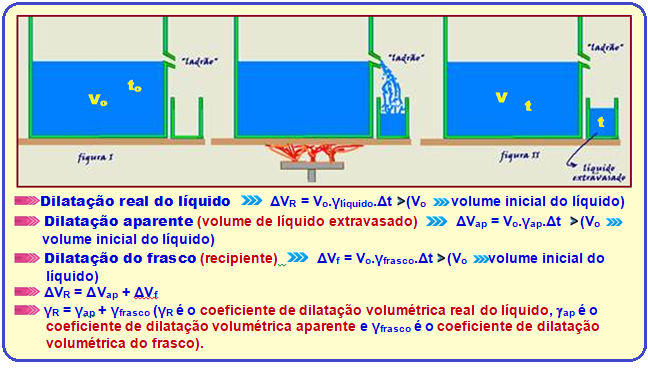
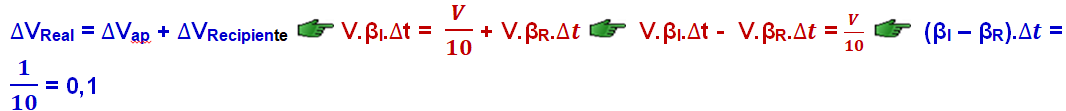
R- D
Termodinâmica
Transformações gasosas
01-(CEDERJ-RJ-2018)

Uma amostra de um gás ideal ocupa, inicialmente, um volume V0, sendo sua temperatura T0 e pressão 3P0.
O gás sofre uma transformação em duas etapas.
Na primeira etapa, a pressão do gás passa de 3P0 para 2P0 mantendo o volume do gás constante igual a V0 e atingindo a temperatura final T1.

Na segunda etapa, o volume do gás muda para 2V0, mantendo pressão do gás constante em 2P0 e atingindo a temperatura final T2.
As relações entre T0, T1 e T2 são:
![]()
02-(UFPR-PR-018)

Em Termodinâmica, estudamos processos importantes que fazem parte de ciclos utilizados em máquinas térmicas, alguns dos quais de grande relevância tecnológica, além de científica.
Com relação ao que ocorre com um gás ideal, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) Em todo processo isovolumétrico, também chamado de isocórico, o trabalho realizado pelo gás é nulo.
( ) Em todo processo adiabático, a energia interna do gás é constante.
( ) Em todo processo isobárico, não há trocas de calor entre o gás e o meio externo.
( ) Em todo processo isotérmico, a temperatura do gás aumenta quando há realização de trabalho sobre ele.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
a) V – V – V – V.
b) F – V – F – F.
c) F – V – F – V.
d) F – F – V – F.
e) V – F – F – F.
03-(Faculdade de Ciências Médicas da Santa Casa de São Paulo – 018)

O gráfico representa parte da curva de aquecimento de determinada massa de gelo, inicialmente a uma temperatura de – 40 oC, até transformar-se em água líquida a 20 oC.
As etapas 1, 2 e 3 indicadas ocorrem em intervalos de tempo ∆t1, ∆t2 e ∆t3, respectivamente.

Considerando que a energia necessária para provocar essa transformação tenha sido fornecida por uma fonte térmica de potência constante, que todo o calor fornecido por essa fonte tenha sido absorvido pela massa que sofreu a transformação, que o calor específico do gelo é 0,5 cal/(g.oC), que o calor específico da água líquida é 1 cal/(g.oC) e que o calor latente de fusão do gelo é 80 cal/g, é correto afirmar que
![]()
04- (PUC-SP-018)


05-Instituto Federal de Educação, Ciência e Tecnologia de Pernambuco – IFPE – 2019

Em uma transformação isobárica, certo gás ideal obedece ao gráfico abaixo. A temperatura,

quando o gás quadruplicar seu volume inicial, será
a) 200K. b) 800K. c) 400K. d) 500K. e) 1000K
06-(UEMA-MA-019)

O gelo seco é gás carbônico (CO2) congelado a uma temperatura superbaixa: -78,5°C. O gás carbônico faz parte do ar que respiramos, além de também ser o ar que soltamos ao expirar. Em quantidades normais, ele não faz mal a nós nem à natureza, muito pelo contrário: ele é responsável por manter a temperatura do planeta, já que, sem ele, seria tudo muito, muito frio.
Um fato curioso sobre o gelo seco é que, quando ele derrete, ele não vira líquido: ele vira um gás.

Isso mesmo: ele vai direto do estado sólido para o estado gasoso. Além disso, depois que ele derreteu, você não consegue dizer que ele estava lá: ele não deixa nenhum cheiro ou resíduo. Mágico, né?
https://blog.tudogostoso.com.br/estilo-de-vida/gelo-seco-como-funciona/
Uma substância pode passar de uma fase para outra, por meio do recebimento ou do fornecimento de calor.
A passagem direta da fase sólida para a gasosa é denominada
a) Fusão.
b) Sublimação.
c) Solidificação.
d) Condensação.
e) Vaporização.
07-(UniCEUB – Medicina – DF – 019)

Uma amostra de gás é contida hermeticamente em um recipiente dotado de êmbolo móvel, ocupando um volume de 1.10-3 m3 , sob temperatura de 200 K e pressão de 2.105 Pa.

O gás passa por uma transformação isobárica que o leva à temperatura de 600 K e, em seguida, por uma transformação isotérmica, de modo que sua pressão passa a ser 3.105 Pa.
No final dos dois processos, o volume do gás será
(A) 2.10-3 m3
(B) 3.10-3 m3
(C) 4.10-3 m3
(D) 5.10-3 m3
(E) 6.10-3 m3
08-(UEMG-MG-019)


09-(Faculdade de Ciências Médicas da Santa Casa de São Paulo – SP – 019)


10-Escola Naval 2018/2019

Analise o diagrama PV abaixo.

A figura acima exibe, num diagrama PV, um ciclo reversível a que está submetido 2 moles de um gás monoatômico ideal. Sabendo que as temperaturas nos estados A, B e C estão relacionadas por TC = 3TB = 9TA, qual a eficiência do ciclo?
(A) 1/3
(B) 1/5
(C) 1/6
(D) 1/7
(E) 1/9
11-(MEDICINA -UNIVERSIDADE MUNICIPAL DE SÃO CAETANO DO SUL –– USCS-SP – 019)

De acordo com o manual técnico de uma panela de pressão caseira, a válvula de segurança da panela será acionada se a pressão no interior desse recipiente atingir 1,80.105 Pa.

Suponha que seja colocado na panela um gás ideal à temperatura de 27 ºC, sob pressão de 1,00. 105 Pa, e que nessa situação o sistema de segurança funcione da forma indicada no manual. A máxima temperatura a que esse gás poderá ser submetido sem que a válvula de segurança da panela seja acionada será
(A) 587 ºC. (B) 127 ºC. (C) 183 ºC. (D) 267 ºC. (E) 330 ºC.
12-Instituto Federal de Educação, Ciência e Tecnologia do Norte de Minas Gerais (IFNMG)- 2019

O ciclo de combustão no cilindro de um motor a álcool pode ser representado – simplificadamente e fora de escala – pelo diagrama da figura.

Nesse diagrama, durante a compressão – no processo de I para F –, o volume da mistura é reduzido de VI para VF.
Nesse caso, sabe-se que a eficiência termodinâmica (E) depende da taxa de compressão e é dada por:

Considerando-se os dados numéricos do diagrama e admitindo-se, numa primeira aproximação, que a mistura ar-álcool comporta-se como um gás ideal, o valor correto de E será:
A) 0,70 B) 0,25 C) 0,40 D) 0,60
13-Instituto Federal de Educação, Ciência e Tecnologia do Norte de Minas Gerais (IFNMG)- 2019

Considere que uma substância S comporta-se segundo o diagrama de fases ilustrado na figura abaixo.

De acordo com esse diagrama, se uma amostra da substância S estiver a 35o C de temperatura e sob pressão de 3,75 atm, o estado de agregação da amostra será:
A) líquido B) vapor C) gás D) sólido
14-(UDESC-SC-019)

Dois moles de gás ideal são comprimidos isotermicamente, à temperatura ambiente de 25ºC, até que o volume deste gás se reduza à metade.
Assinale a alternativa que melhor representa a razão entre as pressões inicial e final do gás.
A. ( ) 2 B. ( ) 4 C. ( ) 1/4 D. ( ) 1 E. ( ) ½
Princípios da Termodinâmica
15-(Universidade Tecnológica Federal do Paraná – UTFPR – 019)

O diagrama a seguir representa a transformação cíclica termodinâmica sofrida por uma massa gasosa:

De acordo com o digrama é correto afirmar que:
A) se o ciclo for percorrido em sentido horário, há conversão de calor em trabalho.
B) ao passar de D para A, o trabalho realizado pelo gás é positivo.
C) ao passar de B para C, o trabalho realizado pelo gás é positivo.
D) a quantidade de calor recebida pelo gás é numericamente igual à área do quadrilátero ABCD.
E) se o ciclo for percorrido em sentido horário, o sistema realiza trabalho sobre o gás.
16-(UFAM-AM-2019)


17-(UFRR-RR-019)


18-(CEDERJ-RJ-2019)

Duas amostras de gás estão em um recipiente rígido isolado termicamente do exterior e com duas câmaras separadas por uma parede que também é rígida. O gás na primeira câmara está a

uma temperatura menor que o gás na segunda câmara. Lentamente, a parede rígida permite a passagem de calor levando a uma situação de equilíbrio térmico entre as câmaras. A variação de energia interna do gás na primeira câmara, ΔU, e o calor recebido por ele, Q, têm seus sinais descritos por
(A) ΔU > 0 e Q > 0 (B) ΔU > 0 e Q < 0 (C) ΔU < 0 e Q > 0 (D) ΔU < 0 e Q < 0
Calor
19-URCA-CE-019)


A)Todo calor produzido pela gasolina é transformado em energia mecânica para movimentar as rodas.
B) O motor de uma moto é considerado uma máquina térmica e somente uma parte do calor gerado é convertido em trabalho mecânico.
C) O fluxo de calor no motor a combustão interna da moto sempre flui da estrutura mais fria para a estrutura mais quente.
D) O rendimento do motor de uma moto pode ser encontrado pela divisão entre a temperatura fria Tfria e a temperatura quente Tquente.
E) A troca de óleo periodicamente garante à eficiência total do funcionamento do motor a combustão interna da moto
20-(UECE-CE-019)

Considere um gás ideal que sofre uma compressão pela realização de trabalho sobre o recipiente

que o contém. Este trabalho tem a mesma unidade de medida de
A) razão entre pressão e volume.
B) produto de pressão por temperatura.
C) razão entre temperatura e pressão.
D) produto de pressão por volume.
21-(EsPCEx- AMAN – SP- RJ – 2018/19)

Considere uma máquina térmica X que executa um ciclo termodinâmico com a realização de

trabalho. O rendimento dessa máquina é de 40% do rendimento de uma máquina Y que funciona
segundo o ciclo de Carnot, operando entre duas fontes de calor com temperaturas de
27 °C e 327 °C. Durante um ciclo, o calor rejeitado pela máquina X para a fonte fria é de 500 J,
então o trabalho realizado neste ciclo é de
[A] 100 J. [B] 125 J. [C] 200 J. [D] 500 J. [E] 625 J.
22- FAMERP – Conhecimentos específicos

Um motor funciona obedecendo ao ciclo de Stirling, no qual um gás ideal é submetido a duas transformações isotérmicas, AB e CD, e a duas transformações isovolumétricas, BC e DA, como mostra a figura.

a) Sabendo que a temperatura do gás na transformação AB é 327 ºC e que a pressão nos pontos B e C valem 8,0 × 105 Pa e 4,0 × 105 Pa, respectivamente, calcule a temperatura do gás, em kelvins, durante a transformação CD.
b) Sabendo que a área S sob a curva da transformação CD, destacada na figura, corresponde a uma quantidade de energia igual a 3700 J, calcule a quantidade de calor, em joules, que o gás libera nessa transformação.
23-(UNESP – SP – 018)

A figura mostra uma máquina térmica em que a caldeira funciona como a fonte quente e o condensador como a fonte fria.

a) Considerando que, a cada minuto, a caldeira fornece, por meio do vapor, uma quantidade de calor igual a 1,6.109 J e que o condensador recebe uma quantidade de calor igual a 1,2.109 J, calcule o rendimento dessa máquina térmica.
b) Considerando que 6,0 × 103 kg de água de refrigeração fluem pelo condensador a cada minuto, que essa água sai do condensador com temperatura 20 ºC acima da temperatura de entrada e que o calor específico da água é igual a 4,0.103 J/(kg⋅ºC), calcule a razão entre a quantidade de calor retirada pela água de refrigeração e a quantidade de calor recebida pelo condensador.
24-(Faculdade de Tecnologia Termomecânica – SP- 018)


25-(UFPR-PR-018)

Em Termodinâmica, estudamos processos importantes que fazem parte de ciclos utilizados em máquinas térmicas, alguns dos quais de grande relevância tecnológica, além de científica.
Com relação ao que ocorre com um gás ideal, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) Em todo processo isovolumétrico, também chamado de isocórico, o trabalho realizado pelo gás é nulo.
( ) Em todo processo adiabático, a energia interna do gás é constante.
( ) Em todo processo isobárico, não há trocas de calor entre o gás e o meio externo.
( ) Em todo processo isotérmico, a temperatura do gás aumenta quando há realização de trabalho sobre ele.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
a) V – V – V – V.
b) F – V – F – F.
c) F – V – F – V.
d) F – F – V – F.
e) V – F – F – F.
26-(UNIFOR-CE-018)

Observa-se um ciclo termodinâmico de um gás ideal apresentado na figura a seguir.

Com relação ao comportamento do gás, é correto afirmar que
(A) no processo BC a temperatura é constante.
(B) o trabalho realizado no processo AB é nulo.
(C) o calor transferido no processo DA é nulo.
(D) o trabalho realizado no processo CD é negativo.
(E) a quantidade de calor no processo CD é igual a variação da energia interna.
27-Universidade Estadual de Ciências da Saúde de Alagoas (UNCISAL-018)



Resolução Comentada – Termodinâmica – 2018-2019
01-
Equação geral dos gases perfeitos


02-

(F) Pelo gráfico o material Y se contrai (volume diminui) quando a temperatura aumenta até 5 oC, e

somente a partir dessa temperatura passa a dilatar-se (volume aumentando).
(V) Veja no gráfico que em T = 5 oC o volume de Y (VY) é menor que o de X (VX).

R- A
03-

04-
Transformação isocórica, isométrica ou isovolumétrica
Nessa transformação o volume é mantido constante (isso=igual; coros=volume).
Os físicos Jacques Charles e Gay-Lussac descobriram experimentalmente que, numa transformação isocórica, a pressão (P) é diretamente proporcional à temperatura absoluta (T), ou seja:

A expressão acima só é válida se considerarmos a temperatura absoluta, isto é, na escala kelvin.
Se a temperatura for medida em graus Celsius, isso não se aplica.
Na expressão Po /To = P/T, conhecida como lei de Charles, Po e To representam a pressão e a temperatura absoluta do gás no estado inicial: P e T representam, respectivamente, a pressão e a temperatura absoluta do gás no estado final.
![]()
Pode-se transformar uma indicação de uma escala para outra conforme o procedimento a seguir,

de acordo com a relação matemática baseada no teorema de Thales.

05-
Transformação isobárica
Ocorre à pressão constante (isso = igual; barros = pressão).
O físico Jacques Charles observou que, para certa massa de gás perfeito, mantida a pressão constante, o volume é diretamente proporcional à temperatura absoluta, ou seja:

A relação acima é denominada lei de Charles e Gay-Lussac para transformações isobáricas e cujo gráfico V x T está representado abaixo:


R- C
06-
Sublimação é um fenômeno físico-químico que consiste na passagem direta de uma substância do estado sólido para o estado gasoso e vice-versa, sem passar pelo estado líquido.
Alguns dos exemplos mais comuns de sublimação são a naftalina, iodo e gelo seco.
R- B
07-
Transformação isobárica


Transformação isotérmica


R- A
08-

 R-
C
R-
C
09-


R- E
10-
Podemos calcular a eficiência η da máquina como a razão entre o trabalho W realizado pela máquina e o calor Q inserido nela:
 O trabalho
realizado se
obtém através da área
compreendida dentro do ciclo triangular,
logo, obtemos o trabalho como
O trabalho
realizado se
obtém através da área
compreendida dentro do ciclo triangular,
logo, obtemos o trabalho como

Já o calor inserido deve ser calculado sobre as trajetórias de A a B e de B a C, pois é onde a temperatura aumenta. Como o gás é ideal e monoatômico, convém relembrar algumas relações para esse tipo de gás utilizando o número de mols n e a constante dos gases ideais R:

11-
A válvula de segurança só será acionada se a temperatura do gás atingir um valor limite T e, até que isso ocorra o volume do gás no interior da panela será constante (transformação isocórica, isométrica ou isovolumétrica).
Transformação isocórica, isométrica ou isovolumétrica


12-

R- A
13-
Diagrama de estado – ponto triplo, tríplice – C)

Veja figura abaixo:

R- A
14-
Transformação isotérmica

Po.Vo =
P.V ![]() Po.Vo =
P.Vo/2
Po.Vo =
P.Vo/2 ![]() Po/P
= 1/2
Po/P
= 1/2
R- E
15-
Primeiro princípio da termodinâmica aplicado numa transformação Cíclica

A alternativa correta é a (A) conforme as informações acima.
R- A
16-
Rendimento de uma máquina térmica de Carnot:

η = 1 – = 1 – = 1 – 0,2 η = 0,8 η = 80%.
R- D
17-
(A) Falsa ► não são equivalentes apesar de serem isotérmica, pois ocorrem a temperaturas diferentes e, em AB recebe energia do meio exterior e em CD cede energia ao meio exterior.
(B) Correta ► a temperatura está aumentando e quando isso acontece a energia interna do sistema aumenta.
(C) Falsa ►o trabalho realizado corresponde à área do ciclo.
(D) Falsa ► são duas isotérmicas e duas isovolumétricas (isocóricas ou isométricas).
(E) Falsa ► a temperatura é constante, mas o volume está aumentando e o gás está recebendo calor.
R- B
18-
Quando dois ou mais corpos que estão a temperaturas diferentes são colocados em contato, ocorrerá uma transferência de energia do corpo de maior temperatura para o corpo de menor temperatura.
Essa transferência de energia ocorre até que os dois corpos tenham a mesma temperatura (mesmo
estado térmico, mesmo nível de vibração das moléculas), estejam numa situação de equilíbrio.
Essa transferência de energia recebe o nome de calor.
Então o gás que está na primeira câmara (menor temperatura) recebe calor da outra de maior

temperatura (Q > 0) e sua energia interna aumenta porque sua variação de temperatura também aumenta (ΔU > 0).
R- A
19-
Segundo Princípio da Termodinâmica

R- B
20-
Veja o formulário abaixo

R- D
21-
Rendimento de uma máquina térmica de Carnot


R- B
22-
a) Por tratar-se de um gás ideal, podemos utilizar a lei de Clapeyron:
![]()
Onde P, V, T e n são, respectivamente, pressão, volume, temperatura e número de mols do gás. R é a constante universal dos gases. Do enunciado e da figura, temos que AB e CD são transformações isotérmicas, DA e BC transformações volumétricas.

Nos pontos B e C os volumes são constantes, fazendo com que a equação de Clapeyron se torne:

Aplicando a relação T/P nos pontos B e C:

Substituindo os valores do enunciado, transformando a temperatura da isotérmica AB de Celsius para Kelvin e sabendo que a curva CD é isotérmica (mesma temperatura):

b) A primeira lei da termodinâmica é dada por:
![]()
Sendo Q a energia fornecida para o gás, W o trabalho exercido pelo gás e a energia interna armazenada pelo gás. Como a curva é isotérmica, deve ser nulo, visto que:
![]()
O trabalho W é dado pela área abaixo da curva no diagrama PxV dada no enunciado, logo, a energia interna é:
![]()
R- D
23-
a)
Fórmulas do rendimento de uma máquina térmica de Carnot

Quantidade
de calor recebido pela fonte fria (condensador) ![]() Q1 =
1,2.109 J.
Q1 =
1,2.109 J.
Quantidade
de calor fornecido pela fonte quente (caldeira) ![]() Q
= 1,6.109 J.
Q
= 1,6.109 J.

24-

25-
(V) Veja informação abaixo:
Transformação isocórica, isométrica ou isovolumétrica
Ocorre
a volume
constante ![]() Vo =
V
Vo =
V ![]() ΔV = 0
ΔV = 0 ![]() W
= P.ΔV
W
= P.ΔV ![]() W = P.0
W = P.0 ![]() W
= 0
W
= 0 ![]() ΔU
= Q – W
ΔU
= Q – W ![]() ΔU = Q – 0
ΔU = Q – 0 ![]() ΔU
= Q
ΔU
= Q


(F) A energia interna (∆U) do gás é igual ao trabalho (W) realizado, com sinal invertido.
Veja informação abaixo:
Transformação adiabática
Nela, o sistema não troca calor com o meio externo (Q = 0) e isso ocorre porque o gás está termicamente isolado ou porque a transformação é muito rápida de modo que qualquer troca de calor com possa ser considerada.
Se
Q = 0 ![]() ΔU
= Q – W
ΔU
= Q – W ![]() ΔU = 0 – W
ΔU = 0 – W ![]() ΔU
= –
W.
ΔU
= –
W.

(F) Há trocas de calor, que é distribuído conforme as informações abaixo:
Transformação isobárica
Ocorre à pressão constante. A variação de temperatura (ΔT) provoca uma variação de energia interna (ΔU) do sistema e a variação de volume (ΔV) produz trabalho.

Parte do calor (Q) recebido pelo sistema é armazenada sob forma de energia interna e parte é transformada em trabalho, de modo que ΔU = Q – W.

(F) Isotérmica ocorre à temperatura constante.
Veja informação abaixo:
Transformação isotérmica
Como a temperatura (T) e a energia interna (U) de um sistema estão associadas à energia cinética das moléculas, se a temperatura for constante (transformação isotérmica), a energia interna (U) do sistema também será constante.
Assim, a variação de energia interna (ΔU) do sistema será nula.
Transformação
isotérmica ![]() ΔU
= 0
ΔU
= 0 ![]() ΔU = Q – W
ΔU = Q – W ![]() 0 = Q – W
0 = Q – W ![]() Q
= W.
Q
= W.

Q
= W ![]() Portanto,
numa transformação
isotérmica (temperatura
constante) todo
calor Q recebido pelo sistema é totalmente transformado em trabalho.
Portanto,
numa transformação
isotérmica (temperatura
constante) todo
calor Q recebido pelo sistema é totalmente transformado em trabalho.
R- E
26-

27-
