Vestibulares Recentes por assunto – FÍSICA TÉRMICA – 2014/2013
Vestibulares Recentes por assunto – 2014/2013
FÍSICA TÉRMICA (TERMOLOGIA)
01-(UFPR-PR-014)

Uma pizza a 185º C foi retirada de um forno quente. Entretanto, somente quando a temperatura

atingir 65º C será possível segurar um de seus pedaços com as mãos nuas, sem se queimar. Suponha que a temperatura T da pizza, em graus Celsius, possa ser descrita em função do tempo t, em minutos, pela expressão T = 160 × 2-0,8xt +25. Qual o tempo necessário para que se possa segurar um pedaço dessa pizza com as mãos nuas, sem se queimar?
![]()
02-(UECE-CE-014)

Considere um gás ideal que passa por dois estados, através de um processo isotérmico reversível. Sobre a pressão P e o volume V desse gás, ao longo desse processo, é correto afirmar-se que
A) PV é crescente de um estado para outro.
B) PV é constante.
C) PV é decrescente de um estado para outro.
D) PV é inversamente proporcional à temperatura do gás.
03-(UEL-PR-014)

Uma gota de álcool de 10 g, à temperatura de 70 ºC, cai em um reservatório com 1000 litros de água a

33 ºC.
Dados: Calor específico da água: 1,0 cal/g ºC
Dados: Calor específico do álcool: 0,6 cal/g ºC
Dados: Massa específica da água: 1000 kg/m3
a) Calcule a quantidade de calor transferida para a água.
b) Calcule a variação de entropia do reservatório de água. Sabendo que ΔS ≥ 0, o que se pode concluir da entropia da gota de álcool?
Apresente os cálculos.
04-(UEA-AM-014)

Um turista estrangeiro leu em um manual de turismo que a temperatura média do estado do Amazonas é de 87,8 graus, medido na escala Fahrenheit. Não tendo noção do que esse valor significa em termos climáticos, o turista consultou um livro de Física, encontrando a seguinte tabela de conversão entre escalas termométricas:

Com base nessa tabela, o turista fez a conversão da temperatura fornecida pelo manual para a escala Celsius e obteve o resultado:
(A) 25. (B) 31. (C) 21. (D) 36. (E) 16.
05-(ACAFE-SC-014)

Com 77% de seu território acima de 300m de altitude e 52% acima de 600m, Santa Catarina figura entre os estados brasileiros de mais forte relevo.
Florianópolis, a capital, encontra-se ao nível do mar.
Lages, no planalto, varia de 850 a 1200 metros acima do nível do mar.
Já o Morro da Igreja situado em Urubici é considerado o ponto habitado mais alto da Região Sul do Brasil.
A tabela abaixo nos mostra a temperatura de ebulição da água nesses locais em função da altitude.

Considere a tabela e os conhecimentos de termologia e analise as afirmações a seguir.
l Em Florianópolis os alimentos preparados dentro da água em uma panela comum são cozidos
mais depressa que em Lages, utilizando-se a mesma panela.
ll No Morro da Igreja, a camada de ar é menor, por consequência, menor a pressão atmosférica
exercida sobre a água, o que implica em um processo de ebulição a uma temperatura inferior a Florianópolis.
lll Se quisermos cozinhar em água algum alimento no Morro da Igreja, em uma panela comum, será
mais difícil que em Florianópolis, utilizando-se a mesma panela. Isso porque a água irá entrar em ebulição e secar antes mesmo que o alimento termine de cozinhar.
lV Se quisermos cozinhar no mesmo tempo em Lages e Florianópolis um mesmo alimento, devemos usar em Florianópolis uma panela de pressão.
Todas as afirmações corretas estão em:
![]()
06-(UNESP-SP-014)

Para testar os conhecimentos de termofísica de seus alunos, o professor propõe um exercício de
calorimetria no qual são misturados 100 g de água líquida a 20 ºC com 200 g de uma liga metálica a 75 ºC. O professor informa que o calor específico da água líquida é 1 cal/(g.ºC) e o da liga é 0,1 cal/
(g.ºX), onde X é uma escala arbitrária de temperatura, cuja relação com a escala Celsius está representada no gráfico.
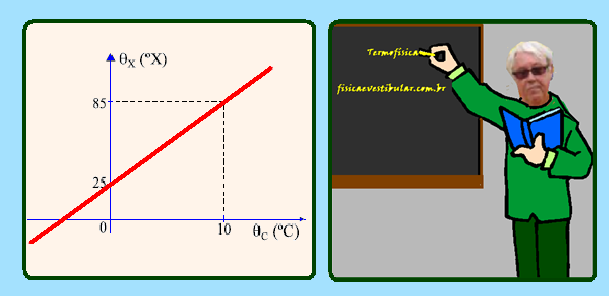
Obtenha uma equação de conversão entre as escalas X e Celsius e, considerando que a mistura seja feita dentro de um calorímetro ideal, calcule a temperatura final da mistura, na escala Celsius, depois de atingido o equilíbrio térmico.
07-(UNESP-SP-014)

Entre 6 e 23 de fevereiro aconteceram os Jogos Olímpicos de Inverno de 2014. Dentre as diversas modalidades esportivas, o curling é um jogo disputado entre duas equipes sobre uma pista de gelo
, seu objetivo consiste em fazer com que uma pedra de granito em forma de disco fique o mais próximo de um alvo circular.
Vassouras são utilizadas pelas equipes para varrer a superfície do gelo na frente da pedra, de modo a influenciar tanto sua direção como sua velocidade.
A intensidade da fricção e a pressão aplicada pelos atletas durante o processo de varredura podem fazer com que a velocidade da pedra mude em até 20% devido à formação de uma película de água líquida entre a pedra e a pista.
O gráfico apresenta o diagrama de fases da água.

Com base nas informações constantes no texto e no gráfico, a seta que representa corretamente a transformação promovida pela varredura é a de número
![]()
08-(UNESP-SP-014)

Foram queimados 4,00 g de carvão até CO2 em um calorímetro.

A temperatura inicial do sistema era de 20,0 ºC e a final, após a combustão, 31,3 ºC. Considere a capacidade calorífica do calorímetro = 21,4 kcal/ºC e despreze a quantidade de calor armazenada na atmosfera dentro do calorímetro. A quantidade de calor, em kcal/g, liberada na queima do carvão,
foi de
![]()
09-(UNESP-SP-014)

O gráfico representa, aproximadamente, como varia a temperatura ambiente no período de um dia, em determinada época do ano, no deserto do Saara. Nessa região a maior parte da superfície do solo é coberta por areia e a umidade relativa do ar é baixíssima.
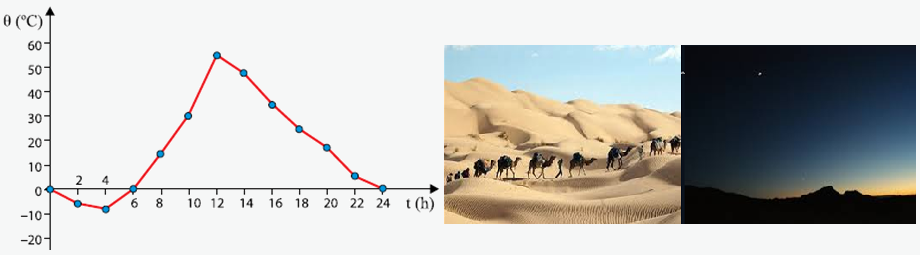
A grande amplitude térmica diária observada no gráfico pode, dentre outros fatores, ser explicada pelo fato de que
(A) a água líquida apresenta calor específico menor do que o da areia sólida e, assim, devido a maior presença de areia do que de água na região, a retenção de calor no ambiente torna-se difícil, causando a drástica queda de temperatura na madrugada.
(B) o calor específico da areia é baixo e, por isso, ela esquenta rapidamente quando ganha calor e esfria rapidamente quando perde. A baixa umidade do ar não retém o calor perdido pela areia quando ela esfria, explicando a queda de temperatura na madrugada.
(C) a falta de água e, consequentemente, de nuvens no ambiente do Saara intensifica o efeito estufa, o que contribui para uma maior retenção de energia térmica na região.
(D) o calor se propaga facilmente na região por condução, uma vez que o ar seco é um excelente condutor de calor. Dessa forma, a energia retida pela areia durante o dia se dissipa pelo ambiente à noite, causando a queda de temperatura.
(E) da grande massa de areia existente na região do Saara apresenta grande mobilidade, causando a dissipação do calor absorvido durante o dia e a drástica queda de temperatura à noite.
10-(FUVEST-SP-014)

Uma lâmina bimetálica de bronze e ferro, na temperatura ambiente, é fixada por uma de suas extremidades, como visto na figura abaixo.
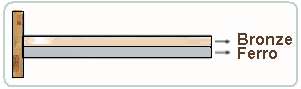
Nessa situação, a lâmina está plana e horizontal. A seguir, ela é aquecida por uma chama de gás. Após algum tempo de aquecimento, a forma assumida pela lâmina será mais adequadamente representada pela figura:


11-(AFA-014)

Um estudante, ao repetir a experiência de James P. Joule para a determinação do equivalente mecânico do calor, fez a montagem da figura abaixo.
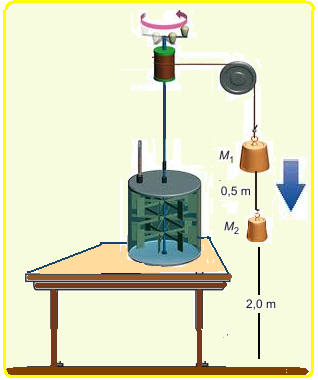
Para conseguir o seu objetivo, ele deixou os corpos de massas M1 = 6,0 kg e M2 = 4,0 kg caírem 40 vezes com velocidade constante de uma altura de 2,0 m, girando as pás e aquecendo 1,0 kg de água contida no recipiente adiabático. Admitindo que toda a variação de energia mecânica ocorrida durante as quedas dos corpos produza aquecimento da água, que os fios e as polias sejam ideais e que o calor específico da água seja igual a 4,0 J/g°C, o aumento de temperatura dela, em °C, foi de
![]()
12-(CEDERJ-RJ-014)

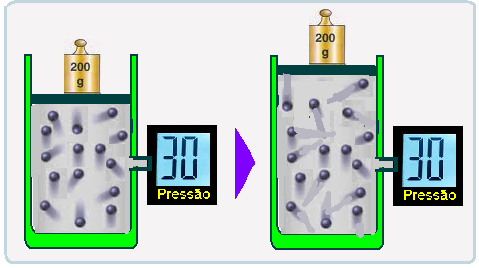
Uma certa quantidade de um gás ideal ocupa a metade esquerda de um recipiente que permite troca de calor com o meio ambiente. Nestas condições, em equilíbrio térmico com o meio ambiente numa temperatura T, observa-se que a pressão do gás é P1. A válvula que mantinha o lado esquerdo (E) do recipiente com gás e o lado direito (D) vazio é aberta. O gás expande-se para todo o recipiente e termina por atingir o equilíbrio térmico com o meio ambiente, na mesma temperatura T.
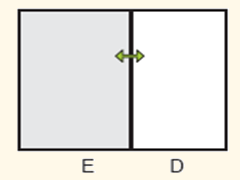
Assinale a alternativa que representa as pressões finais do gás no lado esquerdo, PE, e no lado direito, PD , do recipiente.
![]()
13-(UERJ-RJ-014)

Um sistema é constituído por uma pequena esfera metálica e pela água contida em um reservatório. Na tabela, estão apresentados dados das partes do sistema, antes de a esfera ser inteiramente submersa na água.
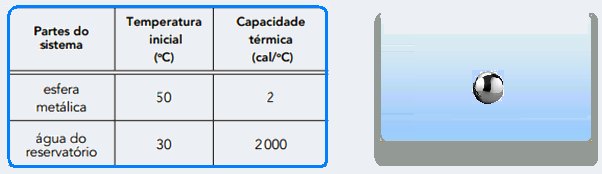
A temperatura final da esfera, em graus Celsius, após o equilíbrio térmico com a água do
reservatório, é cerca de:
(A) 20 (B) 30 (C) 40 (D) 50
14-(UERJ-RJ-014)

Observe na tabela os valores das temperaturas dos pontos críticos de fusão e de ebulição,
respectivamente, do gelo e da água, à pressão de 1 atm, nas escalas Celsius e Kelvin.
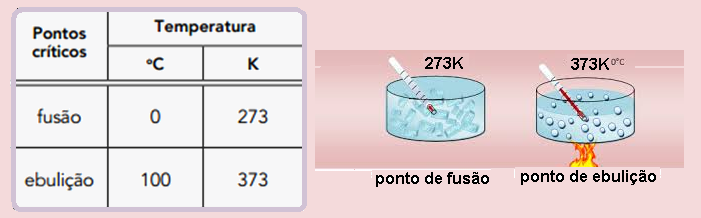
Considere que, no intervalo de temperatura entre os pontos críticos do gelo e da água, o
mercúrio em um termômetro apresenta uma dilatação linear.
Nesse termômetro, o valor na escala Celsius correspondente à temperatura de 313 K é igual a:
![]()
15-(UFSCAR-SP-014)

Uma característica do álcool em seu estado líquido é dada pelo valor numérico 2 400 J/(kg·ºC). Essa

característica é
(A) o calor latente de vaporização, que informa a quantidade de energia térmica necessária para transformar em vapor 1 kg de álcool.
(B) o calor específico, que informa a quantidade de energia térmica necessária para que 1 kg de álcool aumente a temperatura em 1 ºC.
(C) o calor específico, que informa a quantidade de energia térmica contida em uma massa de 2 400 kg de álcool à temperatura de 1 ºC.
(D) o calor latente de condensação, que informa a quantidade de energia térmica necessária para converter em líquido1 kg de álcool.
(E) a capacidade térmica, que relaciona a quantidade de energia térmica recebida pelo álcool e a correspondente variação de temperatura provocada por ele.
16-(FGV-SP-014)

O gráfico da pressão (P), em função do volume (V) de um gás perfeito, representa um ciclo de transformações a que o gás foi submetido.
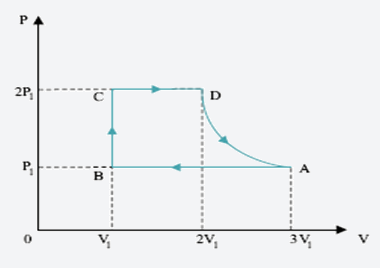
A respeito dessas transformações, é correto afirmar que a transformação
(A) AB é isobárica e que a relação TA/TB entre as temperaturas absolutas nos respectivos estados A e B vale 3.
(B) BC é isotérmica e que a relação TB/TC entre as temperaturas absolutas nos respectivos estados B e C vale 1/2.
(C) CD é isobárica e que a relação TC/TD entre as temperaturas absolutas nos respectivos estados C e D vale 2/3.
(D) AD é isotérmica e que o calor trocado com o meio ambiente nessa transformação é nulo.
(E) AD é adiabática e que o calor trocado com o meio ambiente nessa transformação é igual ao trabalho realizado pelo gás no ciclo.
17-(MACKENZIE-SP-014)

Um internauta, comunicando-se em uma rede social, tem conhecimento de que naquele instante a

temperatura em Nova Iorque é ӨNI = 68 ºF, em Roma é ӨRO = 291 K e em São Paulo, ӨSP = 25 ºC. Comparando essas temperaturas, estabelece-se que
a) ӨNI < ӨRO < ӨSP
b) ӨSP < ӨRO < ӨNI
c) ӨRO < ӨNI < ӨSP
d) ӨRO < ӨSP < ӨNI
e) ӨNI < ӨSP < ӨRO
18-(UDESC-SC-014)

Um sistema fechado, contendo um gás ideal, sofre um processo termodinâmico isobárico,
provocando mudança de temperatura de 200°C para 400°C. Assinale a alternativa que representa a razão aproximada entre o volume final e o inicial do gás ideal.
![]()
19-(UDESC-SC-014)

Certo metal possui um coeficiente de dilatação linear α. Uma barra fina deste metal, de comprimento Lo, sofre uma dilatação para uma dada variação de temperatura ΔT. Para uma chapa quadrada fina de lado Lo e para um cubo também de lado Lo, desse mesmo metal, se a variação de temperatura for 2ΔT, o número de vezes que aumentou a variação da área e do volume, da chapa e do cubo, respectivamente, é:
A. ( ) 4 e 6
B. ( ) 2 e 2
C. ( ) 2 e 6
D. ( ) 4 e 9
E. ( ) 2 e 8
20-(UEL-PR-014)

Em um ambiente com elevado número de indústrias e de circulação de veículos, como as regiões metropolitanas, as partículas em suspensão e os gases poluentes são levados pelas correntes de convecção para as camadas mais altas da atmosfera, onde se dissipam. O fenômeno meteorológico

da inversão térmica, que ocorre geralmente no inverno, tem como consequência o impedimento da dispersão dos poluentes, causando problemas respiratórios na população.
Assinale a alternativa que apresenta, corretamente, a causa da inversão térmica.
a) Uma massa de ar frio ascendente impede o movimento descendente de uma camada de ar quente.
b) Uma massa de ar quente descendente impede o movimento ascendente de uma camada de ar frio.
c) Uma massa de ar frio penetra entre camadas de ar quente, impedindo o movimento descendente do ar.
d) Uma massa de ar quente penetra entre camadas de ar frio, impedindo o movimento descendente do ar.
e) Uma massa de ar quente penetra entre camadas de ar frio, impedindo o movimento ascendente do ar.
Termodinâmica
Instrução: As questões 21 e 22 referem-se aos enunciados e gráfico abaixo.
O gráfico representa, em um processo isobárico, a variação em função do tempo da temperatura de uma amostra de um elemento puro cuja massa é de 1,0 kg, observada durante 9 minutos.
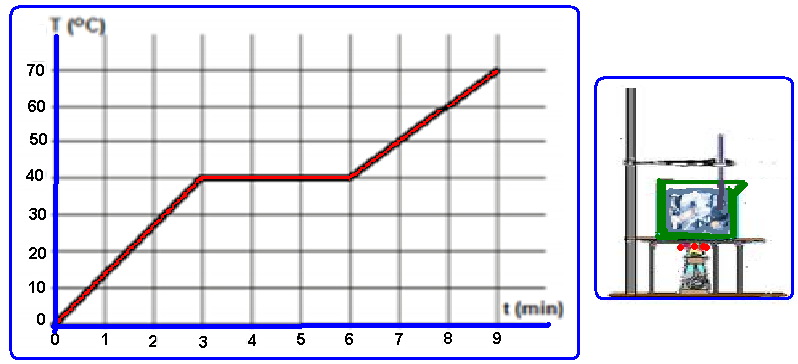
A amostra está no estado sólido a 0o C no instante t=0 e é aquecida por uma fonte de calor que lhe transmite energia a uma taxa de 2,0.103J/min, supondo que não haja perda de calor.
21-(UFRGS-RS-014)

A partir dos dados do gráfico, pode-se afirmar que esse elemento apresenta uma temperatura de fusão e um calor específico no estado líquido que são, respectivamente,
(A) 70º C e 180 J/(kg.K).
(B) 70º C e 200 J/(kg.K).
(C) 40º C e 150 J/(kg.K).
(D) 40º C e 180 J/(kg.K).
(E) 40º C e 200 J/(kg.K).
22-(UFRGS-RS-014)

O processo que ocorre na fase sólida envolve um trabalho total de 0,1 kJ. Nessa fase, a variação da energia interna da amostra é
![]()
23-(UNIFESP-SP-014)

Um gás ideal passa pelo processo termodinâmico representado pelo diagrama P×V. O gás, que se encontrava à temperatura de 57oC no estado inicial A, comprime-se até o estado B, pela perda de 800 J de calor nessa etapa. Em seguida, é levado ao estado final C, quando retorna à temperatura inicial. A linha tracejada representa uma isoterma.
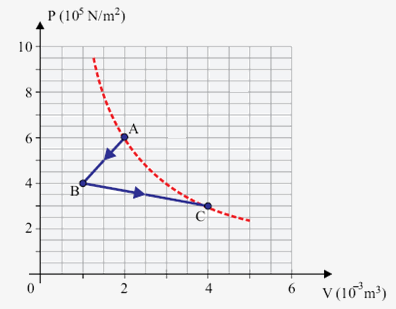
Considerando os valores indicados no gráfico e que a massa do gás tenha permanecido constante durante todo o processo, calcule:
a) a temperatura do gás, em graus Celsius, no estado B.
b) o calor, em joules, recebido pelo gás de uma fonte externa, quando foi levado do estado B para o estado final C.
24-(UNESP-SP-014)

A figura representa um cilindro contendo um gás ideal em três estados, 1, 2 e 3, respectivamente.
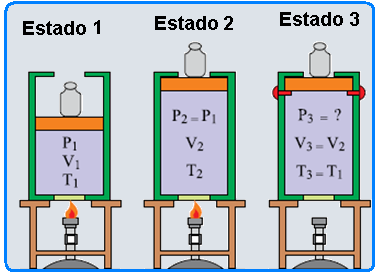
No estado 1, o gás está submetido à pressão P1 = 1,2.105 Pa e ocupa um volume V1 = 0,008 m3 à temperatura T1.
Acende-se uma chama de potência constante sob o cilindro, de maneira que ao receber 500 J de calor o gás sofre uma expansão lenta e isobárica até o estado 2, quando o êmbolo atinge o topo do cilindro e é impedido de continuar a se mover. Nesse estado, o gás passa a ocupar um volume V2 = 0,012 m3 à temperatura T2.
Nesse momento, o êmbolo é travado de maneira que não possa mais descer e a chama é apagada.
O gás é, então, resfriado até o estado 3, quando a temperatura volta ao valor inicial T1 e o gás fica submetido a uma nova pressão P3.
Considerando que o cilindro tenha capacidade térmica desprezível, calcule a variação de energia interna sofrida pelo gás quando ele é levado do estado 1 ao estado 2 e o valor da pressão final P3.
25-(AFA-014)

Dispõe-se de duas máquinas térmicas de Carnot. A máquina 1 trabalha entre as temperaturas de 227 
°C e 527 °C, enquanto a máquina 2 opera entre 227 K e 527 K.
Analise as afirmativas a seguir e responda ao que se pede.
I. A máquina 2 tem maior rendimento que a máquina 1.
II. Se a máquina 1 realizar um trabalho de 2000 J terá retirado 6000 J de calor da fonte quente.
III. Se a máquina 2 retirar 4000 J de calor da fonte quente irá liberar aproximadamente 1720 J de calor para a fonte fria.
IV. Para uma mesma quantidade de calor retirada da fonte quente pelas duas máquinas, a máquina 2 rejeita mais calor para a fonte fria.
São corretas apenas
![]()
26-(UDESC-SC-014)

Analise as duas situações:
I. Um processo termodinâmico adiabático em que a energia interna do sistema cai pela metade.
II. Um processo termodinâmico isovolumétrico em que a energia interna do sistema dobra.
Assinale a alternativa incorreta em relação aos processos termodinâmicos I e II.
A. ( ) Para a situação I o fluxo de calor é nulo, e para a situação II o trabalho termodinâmico é nulo.
B. ( ) Para a situação I o fluxo de calor é nulo, e para a situação II o fluxo de calor é igual à energia interna inicial do sistema.
C. ( ) Para a situação I o trabalho termodinâmico é igual à energia interna inicial do sistema, e para a situação II o fluxo de calor é igual à energia interna final do sistema.
D. ( ) Para a situação I o trabalho termodinâmico é a metade da energia interna inicial do sistema, e para a situação II o trabalho termodinâmico é nulo.
E. ( ) Para ambas situações, a variação da energia interna do sistema é igual ao fluxo de calor menos o trabalho termodinâmico.
27-(UEL-PR-014)

A Revolução Industrial foi acompanhada por profundas transformações na Europa. Os novos meios

de transporte, que utilizavam as máquinas térmicas recém-criadas, foram essenciais aos avanços relacionados à industrialização por todo o continente.
Naquele período, foi demonstrado teoricamente que uma máquina térmica ideal é aquela que descreve um ciclo especial, denominado ciclo de Carnot.
Sobre os princípios físicos da termodinâmica e do ciclo de Carnot, assinale a alternativa correta.
a) As máquinas térmicas, que operam em ciclos, são incapazes de retirar o calor de uma fonte e o transformar integralmente em trabalho.
b) Em uma máquina térmica que opera em ciclos de Carnot, ocorrem duas transformações isobáricas e duas isovolumétricas.
c) No ciclo de Carnot, ocorre uma transformação reversível, enquanto as demais são irreversíveis.
d) O rendimento de uma máquina térmica é nulo quando as etapas do ciclo de Carnot forem transformações reversíveis.
e) Uma máquina térmica é capaz de transferir calor de um ambiente frio para um quente sem a necessidade de consumir energia externa.
Termometria – medida de temperatura
36-(AFA-013)

Dois termômetros idênticos, cuja substância termométrica é o álcool etílico, um deles graduado na

escala Celsius e o outro graduado na escala Fahrenheit, estão sendo usados simultaneamente por um aluno para medir a temperatura de um mesmo sistema físico no laboratório de sua escola. Nessas condições, pode-se afirmar corretamente que
a) os dois termômetros nunca registrarão valores numéricos iguais.
b) a altura da coluna líquida será igual nos dois termômetros, porém com valores numéricos sempre diferentes.
c) a unidade de medida do termômetro graduado na escala Celsius é 1,8 vezes maior que a da escala Fahrenheit.
d) a altura da coluna líquida será diferente nos dois termômetros
37-(ESPEX-013)

Um termômetro digital, localizado em uma praça da Inglaterra, marca a temperatura de 10,4 °F. Essa

temperatura, na escala Celsius, corresponde a
![]()
Propagação do calor
69-(UEL-PR-013)

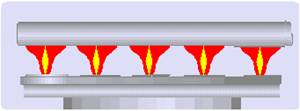
O cooler, encontrado em computadores e em aparelhos eletroeletrônicos, é responsável pelo resfriamento do microprocessador e de outros componentes. Ele contém um ventilador que faz circular ar entre placas difusoras de calor. No caso de computadores, as placas difusoras ficam em contato direto com o processador, conforme a figura a seguir.
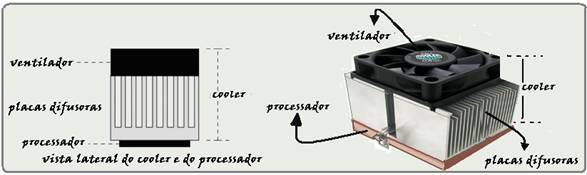
Sobre o processo de resfriamento desse processador, assinale a alternativa correta.
a) O calor é transmitido das placas difusoras para o processador e para o ar através do fenômeno de radiação.
b) O calor é transmitido do ar para as placas difusoras e das placas para o processador através do fenômeno de convecção.
c) O calor é transmitido do processador para as placas difusoras através do fenômeno de condução.
d) O frio é transmitido do processador para as placas difusoras e das placas para o ar através do fenômeno de radiação.
e) O frio é transmitido das placas difusoras para o ar através do fenômeno de radiação.
70-(PUC-GO-013)

A Groenlândia nunca Derreteu Tanto
Texto: No verão da Groenlândia, é normal que suas camadas de gelo se derretam. Em julho de 2012,

no entanto, em apenas quatro dias (de 9 a 12) a superfície gelada sofreu um derretimento nunca observado: a área descongelada passou de 40% para 97%. Apesar de os cientistas definirem o fenômeno como “extremo”, eles explicam que não há motivos para alarde: experimentos apontaram que, nos últimos dez milênios, houve um vasto derretimento a cada 150 anos.
As informações são da Nasa.
(PRADO, Antônio Carlos; DAUDÉN, Laura. A Groenlândia nunca derreteu tanto. Istoé, São paulo, n. 2.229,
p. 28, 27 jul. 2012.)
Sobre esse tema, analise os itens abaixo:
I – Gases de “efeito estufa” contribuem para o aquecimento global por absorver radiação mais infravermelha que visível.
II – A principal fonte de energia da Terra é a radiação.
III – A Superfície do Planeta Terra perde energia para o espaço exterior devido, principalmente, à convecção.
De acordo com os itens analisados, marque a alternativa correta:
A ( ) Apenas I e II são verdadeiros. B ( ) Apenas I e III são verdadeiros.
C ( ) Apenas II e III são verdadeiros. D ( ) I, II e III são verdadeiros.
71-(UNESP-SP-013)

Por que o deserto do Atacama é tão seco?
A região situada no norte do Chile, onde se localiza o deserto do Atacama, é seca por natureza. Ela

sofre a influência do Anticiclone Subtropical do Pacífico Sul (ASPS) e da cordilheira dos Andes.
O ASPS, região de alta pressão na atmosfera, atua como uma “tampa”, que inibe os mecanismos de levantamento do ar necessários para a formação de nuvens e/ou chuva.
Nessa área, há umidade perto da costa, mas não há mecanismo de levantamento. Por isso não chove. A falta de nuvens na região torna mais intensa a incidência de ondas eletromagnéticas vindas do Sol, aquecendo a superfície e elevando a temperatura máxima. De noite, a Terra perde calor mais rapidamente, devido à falta de nuvens e à pouca umidade da atmosfera, o que torna mais baixas as temperaturas mínimas. Essa grande amplitude térmica é uma característica dos desertos.
(Ciência Hoje, novembro de 2012. Adaptado.)
Baseando-se na leitura do texto e dos seus conhecimentos de processos de condução de calor, é correto afirmar que o
ASPS e a escassez de nuvens na região do Atacama .
As lacunas são, correta e respectivamente, preenchidas por
(A) favorece a convecção – favorece a irradiação de calor
(B) favorece a convecção – dificulta a irradiação de calor
(C) dificulta a convecção – favorece a irradiação de calor
(D) permite a propagação de calor por condução – intensifica o efeito estufa
(E) dificulta a convecção – dificulta a irradiação de calor
72-(UNICAMP-SP-013)

A boa ventilação em ambientes fechados é um fator importante para o conforto térmico em regiões de clima quente. Uma chaminé solar pode ser usada para aumentar a ventilação de um edifício. Ela
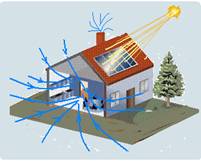
faz uso da energia solar para aquecer o ar de sua parte superior, tornando-o menos denso e fazendo com que ele suba, aspirando assim o ar dos ambientes e substituindo-o por ar vindo do exterior.
a) A intensidade da radiação solar absorvida por uma placa usada para aquecer o ar é igual a 400 W/m2. A energia absorvida durante 1,0 min por uma placa de 2 m2 é usada para aquecer 6,0 kg de ar. O calor específico do ar é c=1000 J/kg.oC.
Qual é a variação de temperatura do ar nesse período?
b) A densidade do ar a 290 K é ρ=1,2 kg/m3 . Adotando-se um número fixo de moles de ar mantido a pressão constante, calcule a sua densidade para a temperatura de 300 K. Considere o ar como um gás ideal.
Termologia
Conceitos iniciais
22-(PUC-MG-013)

O gás de cozinha é constituído principalmente de butano e é comercializado basicamente nos botijões de 13 Kg.
Se se agitar um desses botijões, nota-se que em seu interior existe uma grande quantidade de líquido. Por outro lado, quando os queimadores estão abertos, o que chega aos bicos é material em estado gasoso. Sobre essa situação, é CORRETO afirmar:
a) Quando o butano vai do botijão até os queimadores, ele se aquece e passa do estado líquido para o estado gasoso.
b) Quando o butano está no interior, a pressão sobre ele é suficiente para que a maioria do material se apresente na forma líquida.
c) Na realidade o butano chega aos queimadores no estado líquido e só toma a forma gasosa devido ao calor vindo da queima.
d) O butano só se torna gasoso ao chegar aos queimadores, porque ele é um produto inflamável.
Calorimetria
Calor sensível (específico) e trocas de calor sem mudança de estado
73-(UNIMONTES-MG-013)

Em uma banheira, a temperatura ideal da água para o banho é de 30°C. A banheira está inicialmente
com 25 litros de água a 45°C.
Uma torneira que abastece a banheira tem vazão de 10 litros por minuto. A água da torneira está a 18°C.
As trocas de calor acontecem apenas entre a água da torneira e a água da banheira. O tempo mínimo para que a água da banheira esteja boa para o banho, em segundos, e o volume de água na banheira, em litros, decorrido esse tempo, são, respectivamente:
A) 178,5 e 56,25.
B) 187,5 e 56,52.
C) 187,5 e 56,25.
D) 187,52 e 56,25.
74-(UNIOESTE-PR-013)

Em um recipiente de capacidade térmica desprezível são colocados dois líquidos de calores

específicos c1 e c2 a temperaturas iniciais t1 e t2, respectivamente. Após algum tempo os líquidos, que possuem massas iguais, atingem o equilíbrio térmico.
Considerando a situação descrita, pode-se expressar a temperatura final, tf, da mistura por meio
da equação
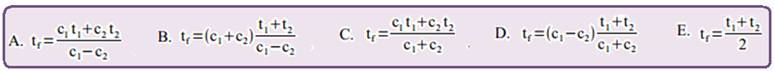
75-(MACKENZIE-SP-013)

Um estudante no laboratório de física, por descuido, colocou 200 g de água liquida (calor específico

1 cal/(g.ºC)) a 100ºC no interior de um calorímetro de capacidade térmica 5 cal/ºC, que contém 100 g de água a 20 ºC.
A massa de água líquida a 0 ºC, que esse aluno deverá adicionar no calorímetro, para que a temperatura de equilíbrio térmico volte a ser 20 ºC, é
a) 900 g b) 800 g c) 700 g d) 600 g e) 500 g
76-(UNICAMP-SP013)

Uma barra cilíndrica é aquecida a uma temperatura de 740°C. Em seguida, é exposta a uma corrente de ar a 40°C.

Sabe-se que a temperatura no centro do cilindro varia de acordo com a função T(t) = (To – Tar).10 – t/12 + Tar, sendo t o tempo em minutos, To a temperatura inicial e Tar a temperatura do ar.
Com essa função, concluímos que o tempo requerido para que a temperatura no centro atinja 140°C é dado pela seguinte expressão, com o log na base 10:
a) 12[log(7) – 1] minutos.
b) 12[1 – log(7)] minutos.
c) 12log(7) minutos.
d) [(1 – log(7)/12 minutos
77- UNICAMP-SP-013)

A boa ventilação em ambientes fechados é um fator importante para o conforto térmico em regiões de clima quente. Uma chaminé solar pode ser usada para aumentar a ventilação de um edifício. Ela

faz uso da energia solar para aquecer o ar de sua parte superior, tornando-o menos denso e fazendo com que ele suba, aspirando assim o ar dos ambientes e substituindo-o por ar vindo do exterior.
a) A intensidade da radiação solar absorvida por uma placa usada para aquecer o ar é igual a 400 W/m2. A energia absorvida durante 1,0 min por uma placa de 2 m2 é usada para aquecer 6,0 kg de ar. O calor específico do ar é c=1000 J/kg.oC. Qual é a variação de temperatura do ar nesse período?
b) A densidade do ar a 290 K é ρ=1,2 kg/m3 . Adotando-se um número fixo de moles de ar mantido a pressão constante, calcule a sua densidade para a temperatura de 300 K. Considere o ar como um gás ideal.
Calor Latente – trocas de calor com mudança de estado
57-(UDESC-SC-013)

Assinale a alternativa que corresponde à temperatura final de equilíbrio quando 10,0g de gelo à

temperatura de -10,0oC são adicionados a 90,0g de água à temperatura de 50,0oC.
Dados: calor específico do gelo — cgelo=0,5cal/goC, calor específico da água — cágua=1 cal/goC, calor latente de fusão do gelo — L=80cal/g
A. ( ) 34,2oC B. ( ) 40,3oC C. ( ) 36,5oC D. ( ) 42,0oC E. ( ) 35,1oC
58-(PUCCAMP-SP-013)

A radiação solar incidente na superfície da Terra provoca a evaporação da água, formando as nuvens.

Esse processo ocorre rapidamente com a água contida em uma panela, aberta à pressão atmosférica normal, ao receber o calor produzido pela combustão do gás de cozinha.
Considere uma porção de 0,50 kg de água, inicialmente a 20 °C, sendo totalmente vaporizada a 100 °C. Seja: cágua=4,2.103J/kgoC e Lvaporização=2,26.106J/kg.
A energia recebida por essa porção de água até a sua vaporização total é, em joules, de
(A) 1,68.103 (B) 2,81.103 (C) 1,13.106 (D) 1,30.106 (E) 2,60.104
59-(PUC-RJ-013)

Três cubos de gelo de 10,0 g, todos eles a 0,0oC, são colocados dentro de um copo vazio e expostos

ao sol até derreterem completamente, ainda a 0,0oC.
Calcule a quantidade total de calor requerida para isto ocorrer, em calorias.
Considere o calor latente de fusão do gelo LF= 80 cal/g
(A) 3,7.101 (B) 2,7.101 (C) 1,1.102 (D) 8,0.102 (E) 2,4.103
60-(MACKENZIR-SP-013)

Uma das características meteorológicas da cidade de São Paulo é a grande diferença de temperatura registrada em um mesmo instante entre diversos pontos do município. Segundo dados do Instituto Nacional de Meteorologia, a menor temperatura registrada nessa cidade foi – 2 ºC, no dia 2 de agosto de 1955, embora haja algumas indicações, não oficiais, de que, no dia 24 de agosto de 1898, registrou-se a temperatura de – 4 ºC.

Em contrapartida, a maior temperatura teria sido 37 ºC, medida em 20 de janeiro de 1999. Considerando-se 100 g de água, sob pressão atmosférica normal, incialmente a – 4 ºC, para chegar a 37 ºC, a quantidade de Energia Térmica que esta massa deverá receber é

a) 11,3 kcal b) 11,5 kcal c) 11,7 kcal d) 11,9 kcal e) 12,1 kcal
61-(UNIFESP-SP-013)

O gráfico representa o processo de aquecimento e mudança de fase de um corpo inicialmente na
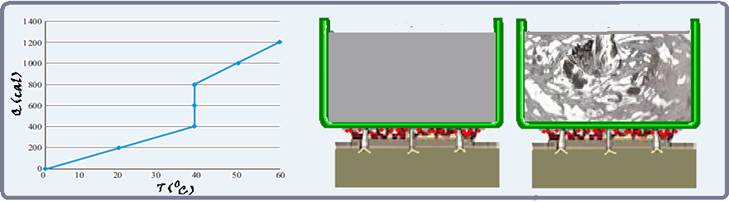
fase sólida, de massa igual a 100 g. Sendo Q a quantidade de calor absorvida pelo corpo, em calorias, e T a temperatura do corpo, em graus Celsius, determine:
a) o calor específico do corpo, em cal/(g ºC), na fase sólida e na fase líquida.
b) a temperatura de fusão, em ºC, e o calor latente de fusão, em cal/g, do corpo.
Dilatometria
Dilatação linear, superficial e volumétrica
78-(UEM-SC-013)

Uma barra homogênea de 50 cm de comprimento e 1 kg de massa, a 20ºC, é constituída por uma
substância de coeficiente de dilatação linear de 2.10-6 ºC-1 e calor específico de 0,5 cal/(gºC).
Uma certa quantidade de calor é fornecida à barra, e sua temperatura é elevada a 50 ºC.
Desprezando as perdas de calor para o meio, analise as alternativas abaixo e assinale o que for correto.
01) A quantidade de calor fornecida à barra é de aproximadamente 1,5.104 cal.
02) A variação do comprimento da barra é de aproximadamente 3.10-3 cm.
04) A capacidade térmica da barra é de aproximadamente 500 cal/ºC.
08) Se o coeficiente de dilatação linear da barra fosse o dobro, a quantidade de calor necessário para variar a
temperatura da barra de 20ºC até 50ºC seria de aproximadamente 3,0.104 cal.
16) A densidade linear de massa da barra permanece perfeitamente inalterada quando a barra é aquecida de 20ºC até 50ºC.
79-(AFA-013)

No gráfico a seguir, está representado o comprimento L de duas barras A e B em função da temperatura θ.

Sabendo-se que as retas que representam os comprimentos da barra A e da barra B são paralelas, pode-se afirmar que a razão entre o coeficiente de dilatação linear da barra A e o da barra B é
a) 2,00. b) 0,50 c) 1,00. d) 0,25.
Termodinâmica
Mudanças de estado físico
52-(UNESP-SP-013)

A liofilização é um processo de desidratação de alimentos que, além de evitar que seus nutrientes saiam junto com a água, diminui bastante sua massa e seu volume, facilitando o armazenamento e o transporte. Alimentos liofilizados também têm seus prazos de validade aumentados, sem perder características como aroma e sabor.

O processo de liofilização segue as seguintes etapas:
I. O alimento é resfriado até temperaturas abaixo de 0 ºC, para que a água contida nele seja solidificada.
II. Em câmaras especiais, sob baixíssima pressão (menores do que 0,006 atm), a temperatura do alimento é elevada, fazendo com que a água sólida seja sublimada.
Dessa forma, a água sai do alimento sem romper suas estruturas moleculares, evitando perdas de proteínas e vitaminas.
O gráfico mostra parte do diagrama de fases da água e cinco processos de mudança de fase, representados pelas setas numeradas de 1 a 5.
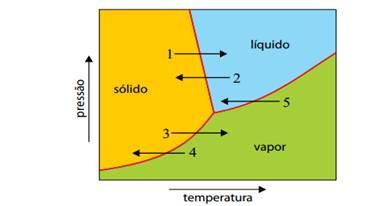
A alternativa que melhor representa as etapas do processo de liofilização, na ordem descrita, é
(A) 4 e 1. (B) 2 e 1. (C) 2 e 3. (D) 1 e 3. (E) 5 e 3.
Transformações gasosas
52-(PUC-RJ-013)

Um sistema termodinâmico recebe certa quantidade de calor de uma fonte quente e sofre uma expansão isotérmica indo do estado 1 ao estado 2, indicados na figura.
Imediatamente após a expansão inicial, o sistema sofre uma segunda expansão térmica, adiabática, indo de um estado 2 para o estado 3 com coeficiente de Poisson λ=1,5.
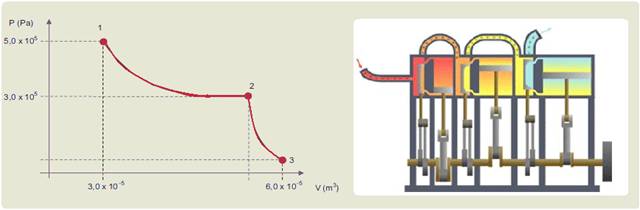
a) Determine o volume ocupado pelo gás após a primeira expansão, indo do estado 1 ao estado 2.
b) Determine a pressão no gás quando o estado 3 é atingido.
53-(PUC-RS-013)

Pode-se escrever a equação geral dos gases na forma P1/T1μ1 = P2/T2μ2 , onde P, T e μ são respectivamente a pressão, a temperatura e a massa específica do gás. A 10km de altitude acima do nível do mar, encontram-se importantes rotas

nível do mar, encontram-se importantes rotas aéreas.
Nessa altitude, a pressão é p2=0,26 atm e a temperatura é T2= -50ºC (223K). Tomando como referência o nível do mar, onde a pressão é p1=1,00 atm e a temperatura é T1=15ºC (288K), e o nível a 10 km de altitude, verifica-se que P2/P1=0,26 e T1/T2≈1,3.
Assim sendo, a razão entre as massas específicas do ar μ2/μ1 nas respectivas altitudes é, aproximadamente,
A) 2,94 B) 2,20 C) 1,00 D) 0,52 E) 0,34
54-(UNESP-SP-013)

A liofilização é um processo de desidratação de alimentos que, além de evitar que seus nutrientes saiam junto com a água, diminui bastante sua massa e seu volume, facilitando o armazenamento e o transporte. Alimentos liofilizados também têm seus prazos de validade aumentados, sem perder características como aroma e sabor.

O processo de liofilização segue as seguintes etapas:
I. O alimento é resfriado até temperaturas abaixo de 0 ºC, para que a água contida nele seja solidificada.
II. Em câmaras especiais, sob baixíssima pressão (menores do que 0,006 atm), a temperatura do alimento é elevada, fazendo com que a água sólida seja sublimada. Dessa forma, a água sai do alimento sem romper suas estruturas moleculares, evitando perdas de proteínas e vitaminas.
O gráfico mostra parte do diagrama de fases da água e cinco processos de mudança de fase, representados pelas setas numeradas de 1 a 5.

A alternativa que melhor representa as etapas do processo de liofilização, na ordem descrita, é
(A) 4 e 1. (B) 2 e 1. (C) 2 e 3. (D) 1 e 3. (E) 5 e 3.
Trabalho de um gás – transformação cíclica
27-(UFV-MG-013)

O gráfico abaixo representa uma transformação cíclica de um gás ideal. É CORRETO afirmar que a
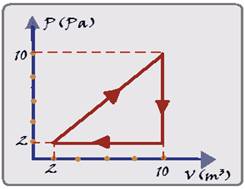
quantidade de calor trocado entre o gás e a sua vizinhança nesse ciclo é:
a) 64 J b) 16 J c) 32 J d) 48 J
28-(UNESP-SP-013)

Determinada massa de gás ideal sofre a transformação cíclica ABCDA mostrada no gráfico. As transformações AB e CD são isobáricas, BC é isotérmica e DA é adiabática.
Considere que, na transformação AB, 400 kJ de calor tenham sidos fornecidos ao gás e que, na transformação CD, ele tenha perdido 440 kJ de calor para o meio externo.
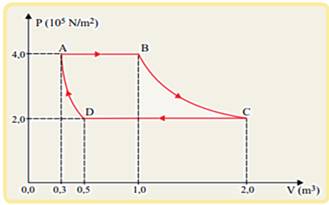
Calcule o trabalho realizado pelas forças de pressão do gás na expansão AB e a variação de energia interna sofrida pelo gás na transformação adiabática DA.
29-(UFV-MG-013)

O gráfico abaixo representa uma transformação cíclica de um gás ideal. É CORRETO afirmar que a

quantidade de calor trocado entre o gás e a sua vizinhança nesse ciclo é:
a) 64 J b) 16 J c) 32 J d) 48 J
Primeiro Princípio da Termodinâmica ou Princípio da Conservação da energia
58-(UFRN-RN-013)

A biomassa é uma das principais fontes de energia renovável e, portanto, máquinas que a utilizam como combustível para geração de energia são importantes do ponto de vista ambiental. Um exemplo bastante comum é o uso da biomassa com o objetivo de acionar uma turbina a vapor para gerar trabalho. A figura ao lado mostra, esquematicamente, uma usina termoelétrica simplificada.
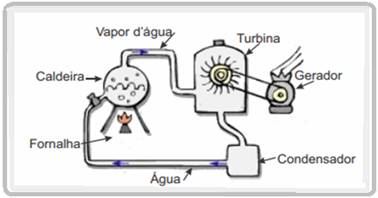
Nessa termoelétrica, a queima da biomassa na fornalha produz calor, que aquece a água da caldeira e gera vapor a alta pressão.
O vapor, por sua vez, é conduzido por tubulações até a turbina que, sob a ação deste, passa a girar suas pás.
Considere desprezíveis as perdas de calor devido às diferenças de temperatura entre as partes dessa máquina térmica e o ambiente. Nesse contexto, a variação da energia interna da água da caldeira
A) é maior que a soma do calor a ela fornecido pela queima da biomassa com o trabalho realizado sobre a turbina.
B) é igual à soma do calor a ela fornecido pela queima da biomassa com o trabalho realizado sobre a turbina.
C) é igual à diferença entre o calor a ela fornecido pela queima da biomassa e o trabalho realizado sobre a turbina.
D) é maior que a diferença entre calor a ela fornecido pela queima da biomassa e o trabalho realizado sobre a turbina.
59-(UNESP-SP-013)

Determinada massa de gás ideal sofre a transformação cíclica ABCDA mostrada no gráfico. As transformações AB e CD são isobáricas, BC é isotérmica e DA é adiabática. Considere que, na transformação AB, 400 kJ de calor tenham sidos fornecidos ao gás e que, na transformação CD, ele tenha perdido 440 kJ de calor para o meio externo.

Calcule o trabalho realizado pelas forças de pressão do gás na expansão AB e a variação de energia interna sofrida pelo gás na transformação adiabática DA.
Segunda lei da Termodinâmica
49-(ENEM-MEC-012)

Aumentar a eficiência na queima de combustível dos motores a combustão e reduzir suas emissões
de poluentes é a meta de qualquer fabricante de motores. É também o foco de uma pesquisa brasileira que envolve experimentos com plasma, o quarto estado da matéria e que está presente no processo de ignição.
A interação da faísca emitida pela vela de ignição com as moléculas de combustível gera o plasma que provoca a explosão liberadora de energia que, por sua vez, faz o motor funcionar. Disponível em: www.inovacaotecnologica.com.br. Acesso em: 22 jul. 2010 (adaptado).
No entanto, a busca da eficiência referenciada no texto apresenta como fator limitante
a) o tipo de combustível, fóssil, que utilizam. Sendo um insumo não renovável, em algum momento estará esgotado.
b) um dos princípios da termodinâmica, segundo o qual o rendimento de uma máquina térmica nunca atinge o ideal.
c) o funcionamento cíclico de todos os motores. A repetição contínua dos movimentos exige que parte da energia seja transferida ao próximo ciclo.
d) as forças de atrito inevitável entre as peças. Tais forças provocam desgastes contínuos que com o tempo levam qualquer material à fadiga e ruptura.
e) a temperatura em que eles trabalham. Para atingir o plasma, é necessária uma temperatura maior que a de fusão do aço com que se fazem os motores.
50-(UFV-MG-013)

As afirmativas abaixo comparam o rendimento de duas máquinas térmicas. Analise cada uma das,
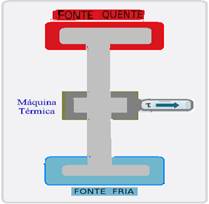
afirmativas, atribuindo V para as verdadeiras e F para as falsas:
( ) A máquina que tem o maior rendimento é a que produz a maior quantidade de trabalho.
( ) Se as duas máquinas produzem a mesma quantidade de trabalho, a que tem o maior rendimento é a que gastou o menor tempo para produzir tal trabalho.
( ) A máquina que tem o maior rendimento é a que retira a menor quantidade de calor do reservatório quente.
Assinale a sequência CORRETA:
a) F, V, F. b) V, F, V. c) F, F, F. d) V, V, V.
51-(FMABC-SP-013)

Determinada máquina térmica foi projetada para operar realizando o ciclo de Carnot. Quando em operação, o trabalho útil fornecido pela máquina, a cada ciclo, é de 3200J. As temperaturas das fontes térmicas são 427°C e 77°C, respectivamente.
Nestas condições, a quantidade de calor retirada da fonte quente, a quantidade de calor rejeitada para a fonte fria e o rendimento da máquina térmica são, respectivamente, iguais a:
Adote 4J = 1cal
(A) 3900J, 700J, 82%
(B) 6400J, 3200J, 50%
(C) 3200J, 6400J, 50%
(D) 700J, 3900J, 82%
(E) 1600J, 3200J, 50%
